Related Articles
- 27 Nov 18Depuis quelques décennies, on a vu la communauté médicale et sanitaire recommander au grand public de « boire avec modération ». De récentes découvertes scientifiques rendent pourtant difficile à tout médecin raisonnable de maintenir cette position. Il est peut-être temps pour la communauté médicale d’en finir avec cette recommandation inutile et nocive, et de soutenir la cause de l’abstinence plutôt que celle de la modération.
- 21 Mai 18Le magnésium est le quatrième minéral le plus abondant dans le corps humain,[1] et il est essentiel à plusieurs centaines de réactions métaboliques et hormonales, chaque jour.[2] Il participe à la formation osseuse (avec le calcium) et ses propriétés myorelaxantes naturelles favorisant le sommeil en font l'objet d'un intérêt croissant. Mais ce n'est qu'un aperçu des bienfaits du magnésium. Il est nécessaire pour le fonctionnement normal des nerfs et des muscles, le rythme cardiaque et la santé du système immunitaire.
- 02 Sept 16
- 07 Mai 15
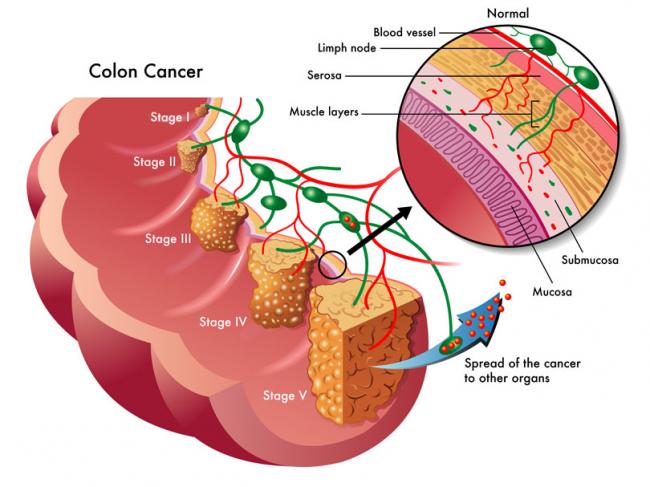
- 18 Avr 16En 2015, 1 homme sur 14 et 1 femme sur 16 ont été diagnostiqués comme souffrant d’un cancer colorectal. Il s’agit de la deuxième cause de décès par cancer pour les hommes, avec 1 chance sur 29 d’en mourir, et de la troisième cause de décès par cancer pour les femmes.
- 14 Janv 17
- 08 Janv 15
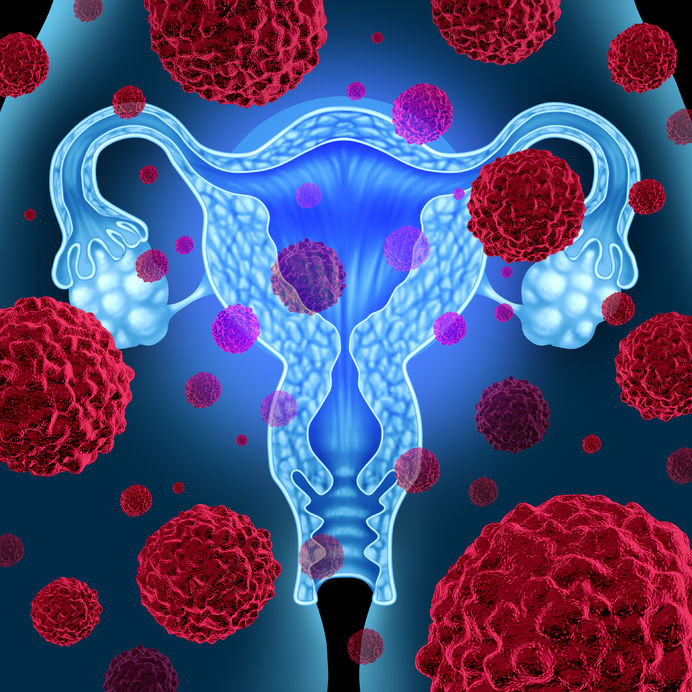
 Le terme dysplasie cervicale se réfère aux cellules anormales présentes sur la surface du col de l’utérus considérées précancéreuses et pouvant mener au cancer. 1) La dysplasie cervicale est principalement causée par une infection transmise sexuellement aux différentes souches du virus du papillome humain (VPH). Des souches différentes peuvent être impliquées autant dans les lésions bénignes que malignes, ce qui signifie que la progression de la maladie semble être dépendante de facteurs individuels. Les études suggèrent qu’une exposition au VPH est l’événement initiateur pouvant entrainer le développement de la dysplasie cervicale, aussi nommée néoplasie intraépithéliale cervicale (CIN).
Le terme dysplasie cervicale se réfère aux cellules anormales présentes sur la surface du col de l’utérus considérées précancéreuses et pouvant mener au cancer. 1) La dysplasie cervicale est principalement causée par une infection transmise sexuellement aux différentes souches du virus du papillome humain (VPH). Des souches différentes peuvent être impliquées autant dans les lésions bénignes que malignes, ce qui signifie que la progression de la maladie semble être dépendante de facteurs individuels. Les études suggèrent qu’une exposition au VPH est l’événement initiateur pouvant entrainer le développement de la dysplasie cervicale, aussi nommée néoplasie intraépithéliale cervicale (CIN). - 03 Janv 14
 La vitamine D3, aussi connue sous le nom de cholécalciférol ou la « vitamine du soleil » est un nutriment en pleine émergence offrant un éventail de rôles thérapeutiques potentiels. En plus d’être bien reconnue pour son rôle dans la santé osseuse, la vitamine D est analysée comme agent important dans la modulation de la fonction immunitaire, des émotions et des fonctions cognitives ainsi que pour son impact sur les facteurs de risque cardiovasculaire et ses effets protecteurs contre le développement du cancer .
01 Déc 13
La vitamine D3, aussi connue sous le nom de cholécalciférol ou la « vitamine du soleil » est un nutriment en pleine émergence offrant un éventail de rôles thérapeutiques potentiels. En plus d’être bien reconnue pour son rôle dans la santé osseuse, la vitamine D est analysée comme agent important dans la modulation de la fonction immunitaire, des émotions et des fonctions cognitives ainsi que pour son impact sur les facteurs de risque cardiovasculaire et ses effets protecteurs contre le développement du cancer .
01 Déc 13 L’incidence réfère au nombre de nouveaux cas d’une maladie ou condition en particulier répertoriée au cours d’une année donnée. L’information qui suit est tirée de la publication Statistiques canadiennes sur le cancer, publiée conjointement par la Société canadienne du cancer et par Statistiques Canada. En général, l’incidence a augmenté lentement au Canada, ce qui peut être en théorie expliqué par à une meilleure détection et par une population vieillissante plutôt qu’à un risque plus élevé de cancer.
03 Janv 14
L’incidence réfère au nombre de nouveaux cas d’une maladie ou condition en particulier répertoriée au cours d’une année donnée. L’information qui suit est tirée de la publication Statistiques canadiennes sur le cancer, publiée conjointement par la Société canadienne du cancer et par Statistiques Canada. En général, l’incidence a augmenté lentement au Canada, ce qui peut être en théorie expliqué par à une meilleure détection et par une population vieillissante plutôt qu’à un risque plus élevé de cancer.
03 Janv 14 Le curcuma est une épice utilisée dans la cuisine Sud-Orientale et celle du Moyen-Orient. De surcroît à son statut d’épice populaire, il s’agit d’une herbe importante dans plusieurs disciplines de médecine. L’usage médicinal du curcuma remonte à 4000 ans en Inde. On l’appelle de bien des noms : le safran indien, le haldi, rhizoma curcumae (jiang huang), asterre merite. Certains le prénomment la racine jaune car le rhizome (racine) de la plante Curcuma longa est jaune.10 Févr 14
Le curcuma est une épice utilisée dans la cuisine Sud-Orientale et celle du Moyen-Orient. De surcroît à son statut d’épice populaire, il s’agit d’une herbe importante dans plusieurs disciplines de médecine. L’usage médicinal du curcuma remonte à 4000 ans en Inde. On l’appelle de bien des noms : le safran indien, le haldi, rhizoma curcumae (jiang huang), asterre merite. Certains le prénomment la racine jaune car le rhizome (racine) de la plante Curcuma longa est jaune.10 Févr 14 Le resvératrol est un phytonutriment et antioxydant important disponible naturellement dans la peau des raisins rouges, des arachides et de certaines baies(1) — il est également prôné comme composante santé que l’on retrouve dans le vin rouge. Au cours des dernières années, la recherche portant sur le resvératrol a pris beaucoup d’ampleur. 17 juin 16
Le resvératrol est un phytonutriment et antioxydant important disponible naturellement dans la peau des raisins rouges, des arachides et de certaines baies(1) — il est également prôné comme composante santé que l’on retrouve dans le vin rouge. Au cours des dernières années, la recherche portant sur le resvératrol a pris beaucoup d’ampleur. 17 juin 16 L’usage des médecines complémentaires pour le traitement du cancer et ses effets secondaires est monté en flèche ces dernières années. Les thérapies complémentaires, de nature non pharmaceutique, améliorent la qualité de vie et réduisent les effets secondaires des thérapies conventionnelles. Elles comprennent le massage, le yoga, la méditation, l’acuponcture, la supplémentation nutritionnelle et les thérapies intraveineuses.22 Avr 16Toutes les femmes – pourvu qu’elles vivent assez longtemps – connaitront la ménopause. Pour certaines, la transition se passe bien, et peut même être vécue comme un soulagement vis-à-vis des soucis du cycle menstruel. Pour d’autres, le changement se révèle très éprouvant car elles doivent faire avec de fréquentes bouffées de chaleur, une prise de poids et une grave dépression. Beaucoup des symptômes de la ménopause peuvent être directement reliés à la réduction de la production des hormones sexuelles, en particulier l’œstrogène et la progestérone.26 Août 13
L’usage des médecines complémentaires pour le traitement du cancer et ses effets secondaires est monté en flèche ces dernières années. Les thérapies complémentaires, de nature non pharmaceutique, améliorent la qualité de vie et réduisent les effets secondaires des thérapies conventionnelles. Elles comprennent le massage, le yoga, la méditation, l’acuponcture, la supplémentation nutritionnelle et les thérapies intraveineuses.22 Avr 16Toutes les femmes – pourvu qu’elles vivent assez longtemps – connaitront la ménopause. Pour certaines, la transition se passe bien, et peut même être vécue comme un soulagement vis-à-vis des soucis du cycle menstruel. Pour d’autres, le changement se révèle très éprouvant car elles doivent faire avec de fréquentes bouffées de chaleur, une prise de poids et une grave dépression. Beaucoup des symptômes de la ménopause peuvent être directement reliés à la réduction de la production des hormones sexuelles, en particulier l’œstrogène et la progestérone.26 Août 13 Nous vivons dans une société où de 10 à 37% de la population adulte souffre d’insomnie, un problème qui affecte la performance psychomotrice chez les individus, entraine la somnolence, les accidents et les troubles de mémoire.(1,2) Ces individus peuvent être généralement catégorisés dans une des trois catégories : ceux ayant de la difficulté à s’endormir, ceux ayant de la difficulté à demeurer endormis et tous deux combinés.01 juil 13
Nous vivons dans une société où de 10 à 37% de la population adulte souffre d’insomnie, un problème qui affecte la performance psychomotrice chez les individus, entraine la somnolence, les accidents et les troubles de mémoire.(1,2) Ces individus peuvent être généralement catégorisés dans une des trois catégories : ceux ayant de la difficulté à s’endormir, ceux ayant de la difficulté à demeurer endormis et tous deux combinés.01 juil 13 C’est un sujet peu populaire, mais la santé de la prostate ou plutôt la mauvaise santé de cette dernière affecte la plupart des hommes lorsqu’ils approchent de l’âge de 50 ans ou plus. Il est dur de croire que ce petit organe, pas plus gros qu’une noix de Grenoble, peut être si important. Les maladies de la prostate se catégorisent dans deux groupes : les maladies de la prostate bénignes et le cancer de la prostate.23 Mars 15Le cancer de la prostate est le cancer le plus fréquent chez les hommes au Canada (à l’exclusion du cancer de la peau sans mélanome). On prévoit qu’un Canadien sur 8 développera la maladie au cours de sa vie, et qu’un sur 28 en mourra (1). Au Canada, le taux de survie à cinq ans pour le cancer de la prostate est de 96% ; mais en dépit de cette statistique positive, une moyenne de 65 Canadiens reçoivent chaque jour un diagnostic de cancer de la prostate, et 11 en meurent (1). Selon la Société canadienne du cancer, le taux d'incidence du cancer de la prostate a augmenté depuis 1980, ce qui peut être dû en partie au vieillissement de la population, à la diminution du PSA (antigène prostatique spécifique, qui mesure la santé de la prostate) au profit de la biopsie, au dépistage plus systématique et à une meilleure sensibilité de la biopsie de la prostate (2).23 Mars 15L’Origanum vulgare (nom latin de l’origan) a fait l’objet de nombreuses études en raison de ses usages cliniques potentiels tout à la fois intéressants et stimulants, et peut-être aussi du fait de la tendance actuelle, dans plusieurs secteurs industriels, à remplacer les substances chimiques de synthèse par des produits naturels aux propriétés similaires. Beaucoup de composants bioactifs sont présents dans les plantes aromatiques et peuvent en être extraits de plusieurs façons. Les principaux composants de l’huile essentielle d’origan mis en évidence par une étude sont le carvacrol, l’alcool bêta-fenchyl, le thymol et le gamma-terpinène (1).23 Févr 15Apprendre que l’on a un cancer est sans aucun doute de nature à bouleverser la vie, et peut provoquer plus d’angoisse que tout autre diagnostic. Les patients peuvent craindre pour leur vie, craindre de l’annoncer à leur famille, à leurs amis et à leurs collègues, et craindre aussi ce que sera le traitement. Tout cela a un impact psychologique énorme, qui va augmenter considérablement le niveau de stress.Quercétine - Composé provenant de fruits et légumes ayant de nombreux effets bénéfiques sur la santé27 juin 14La quercétine fait partie de la famille des flavonoïdes. Les flavonoïdes, parfois appelés bioflavonoïdes, font partie des éléments qui donnent leur couleur aux fruits et aux légumes. La quercétine est plus spécifiquement un flavonol, une sous-classe des flavonoïdes. Il y a beaucoup de sous-classes parmi les flavonoïdes, et beaucoup de composés dans chacune d'entre elles. La quercétine est un de ces composés, dans la sous-classe des flavonols. Les composés de chaque sous-classe ont une structure chimique similaire. Ce n'est un secret pour personne qu'une alimentation riche en fruits et légumes est associée à une meilleure santé et un risque réduit de maladie chronique [1].22 Oct 15Nous sommes tous coupables. Oui, vous aussi. Vous savez de quoi je parle ? De l’hygiène personnelle. Ne vous méprenez pas : le but de cet article n’est pas de vous convaincre que l’hygiène est une mauvaise chose, et de vous faire honte de vous laver les cheveux ou de vous brosser les dents. Je veux juste attirer votre attention sur le fait que la plupart des produits que nous utilisons pour rester propres et agréables à regarder pourraient avoir un sérieux impact sur notre santé.
C’est un sujet peu populaire, mais la santé de la prostate ou plutôt la mauvaise santé de cette dernière affecte la plupart des hommes lorsqu’ils approchent de l’âge de 50 ans ou plus. Il est dur de croire que ce petit organe, pas plus gros qu’une noix de Grenoble, peut être si important. Les maladies de la prostate se catégorisent dans deux groupes : les maladies de la prostate bénignes et le cancer de la prostate.23 Mars 15Le cancer de la prostate est le cancer le plus fréquent chez les hommes au Canada (à l’exclusion du cancer de la peau sans mélanome). On prévoit qu’un Canadien sur 8 développera la maladie au cours de sa vie, et qu’un sur 28 en mourra (1). Au Canada, le taux de survie à cinq ans pour le cancer de la prostate est de 96% ; mais en dépit de cette statistique positive, une moyenne de 65 Canadiens reçoivent chaque jour un diagnostic de cancer de la prostate, et 11 en meurent (1). Selon la Société canadienne du cancer, le taux d'incidence du cancer de la prostate a augmenté depuis 1980, ce qui peut être dû en partie au vieillissement de la population, à la diminution du PSA (antigène prostatique spécifique, qui mesure la santé de la prostate) au profit de la biopsie, au dépistage plus systématique et à une meilleure sensibilité de la biopsie de la prostate (2).23 Mars 15L’Origanum vulgare (nom latin de l’origan) a fait l’objet de nombreuses études en raison de ses usages cliniques potentiels tout à la fois intéressants et stimulants, et peut-être aussi du fait de la tendance actuelle, dans plusieurs secteurs industriels, à remplacer les substances chimiques de synthèse par des produits naturels aux propriétés similaires. Beaucoup de composants bioactifs sont présents dans les plantes aromatiques et peuvent en être extraits de plusieurs façons. Les principaux composants de l’huile essentielle d’origan mis en évidence par une étude sont le carvacrol, l’alcool bêta-fenchyl, le thymol et le gamma-terpinène (1).23 Févr 15Apprendre que l’on a un cancer est sans aucun doute de nature à bouleverser la vie, et peut provoquer plus d’angoisse que tout autre diagnostic. Les patients peuvent craindre pour leur vie, craindre de l’annoncer à leur famille, à leurs amis et à leurs collègues, et craindre aussi ce que sera le traitement. Tout cela a un impact psychologique énorme, qui va augmenter considérablement le niveau de stress.Quercétine - Composé provenant de fruits et légumes ayant de nombreux effets bénéfiques sur la santé27 juin 14La quercétine fait partie de la famille des flavonoïdes. Les flavonoïdes, parfois appelés bioflavonoïdes, font partie des éléments qui donnent leur couleur aux fruits et aux légumes. La quercétine est plus spécifiquement un flavonol, une sous-classe des flavonoïdes. Il y a beaucoup de sous-classes parmi les flavonoïdes, et beaucoup de composés dans chacune d'entre elles. La quercétine est un de ces composés, dans la sous-classe des flavonols. Les composés de chaque sous-classe ont une structure chimique similaire. Ce n'est un secret pour personne qu'une alimentation riche en fruits et légumes est associée à une meilleure santé et un risque réduit de maladie chronique [1].22 Oct 15Nous sommes tous coupables. Oui, vous aussi. Vous savez de quoi je parle ? De l’hygiène personnelle. Ne vous méprenez pas : le but de cet article n’est pas de vous convaincre que l’hygiène est une mauvaise chose, et de vous faire honte de vous laver les cheveux ou de vous brosser les dents. Je veux juste attirer votre attention sur le fait que la plupart des produits que nous utilisons pour rester propres et agréables à regarder pourraient avoir un sérieux impact sur notre santé.
Actualités
Votre abonnement n'a pas pu être enregistré. Veuillez réessayer.
Vous vous êtes abonné avec succès à l’infolettre de Naturopathic Currents.
Les plus populaires
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13