www.naturopathicfoundations.ca
aregina@naturopathicfoundations.ca
Le tractus gastro-intestinal (TGI) humain contient à lui seul 1014 micro-organismes incluant des bactéries, des virus et des fungi.[1] Cela représente à peu près 100 fois plus de cellules microbiennes que de cellules humaines, ce qui nous montre à quel point elles peuvent affecter la santé humaine[2]. Le terme que l’on utilise pour décrire l’étendue de micro-organismes que l’on trouve dans un environnement est « microbiote »[3]. L’environnement dans lequel ces organismes vivent est appelé le « microbiome »[4], dans le cas présent, il s’agit du TGI humain. Les humains et les micro-organismes ont évolué ensemble au fil du temps, formant une relation symbiotique et mutuellement bénéfique[5]. Le microbiote intestinal confère un certain nombre d’avantages. Il assure notamment le maintien de l’intégrité de la barrière muqueuse du TGI, mais aussi la production de vitamines et de nutriments, ainsi que la régulation du système immunitaire[6]. Il y a un équilibre optimal dans le TGI ; toute perturbation de cet équilibre peut déclencher une panoplie de symptômes, car certains micro-organismes peuvent avoir des effets néfastes sur le corps et peuvent contribuer au développement de maladies[7]. Cela s’appelle la « dysbiose »[8].
Les maladies concernées par une dysbiose intestinale
Maladies inflammatoires des intestins (MII)
Le terme de maladies inflammatoires des intestins (MII) fait référence à un groupe de maladies dont les deux formes principales sont la maladie de Chron et la colite ulcéreuse. Ces deux pathologies impliquent une inflammation résultant sur des lésions dans l’appareil digestif, ce qui entraine des douleurs abdominales, des carences en nutriments et une affection générale. La dysbiose peut à la fois être la cause et le résultat d’une MII[9]. En cas de MII, le système immunitaire devient extrêmement agressif à l’intérieur de l’appareil digestif, ce qui entraine une inflammation. Le système immunitaire attaque également certains micro-organismes, ce qui est attesté par le fait que la diversité microbienne observée chez les personnes atteintes de MII est réduite[10]. Les organismes protecteurs comme les Bifidobacterium et les Clostridium sont en quantités réduites, tandis que les espèces destructives comme les Proteobacteria et certaines souches d’E. coli sont en augmentation.[11] Ces espèces destructives encouragent encore plus l’inflammation et activent des réponses immunitaires qui déclenchent des maladies[12].
La dépression
L’axe cerveau-intestins-microbiote est bidirectionnel[13]. Le cerveau communique avec les intestins et les microbes qui se trouvent dans les intestins peuvent communiquer avec le cerveau[14]. La voie de communication centrale est impliquée par le biais du nerf vague, qui connecte directement le TGI au cerveau[15]. L’inflammation est une des caractéristiques de la dépression et peut altérer le fonctionnement de la barrière intestinale, ce qui induit des changements au niveau des bactéries intestinales[16]. Les patients souffrant de dépression ont notamment un microbiote différent avec des niveaux réduits de bactéries bénéfiques par rapport aux personnes non-dépressives[17]. Cette dysbiose contribue à renforcer les symptômes de la dépression, car les bactéries qui communiquent avec le cerveau sont proinflammatoires[18] et le cycle se poursuit.
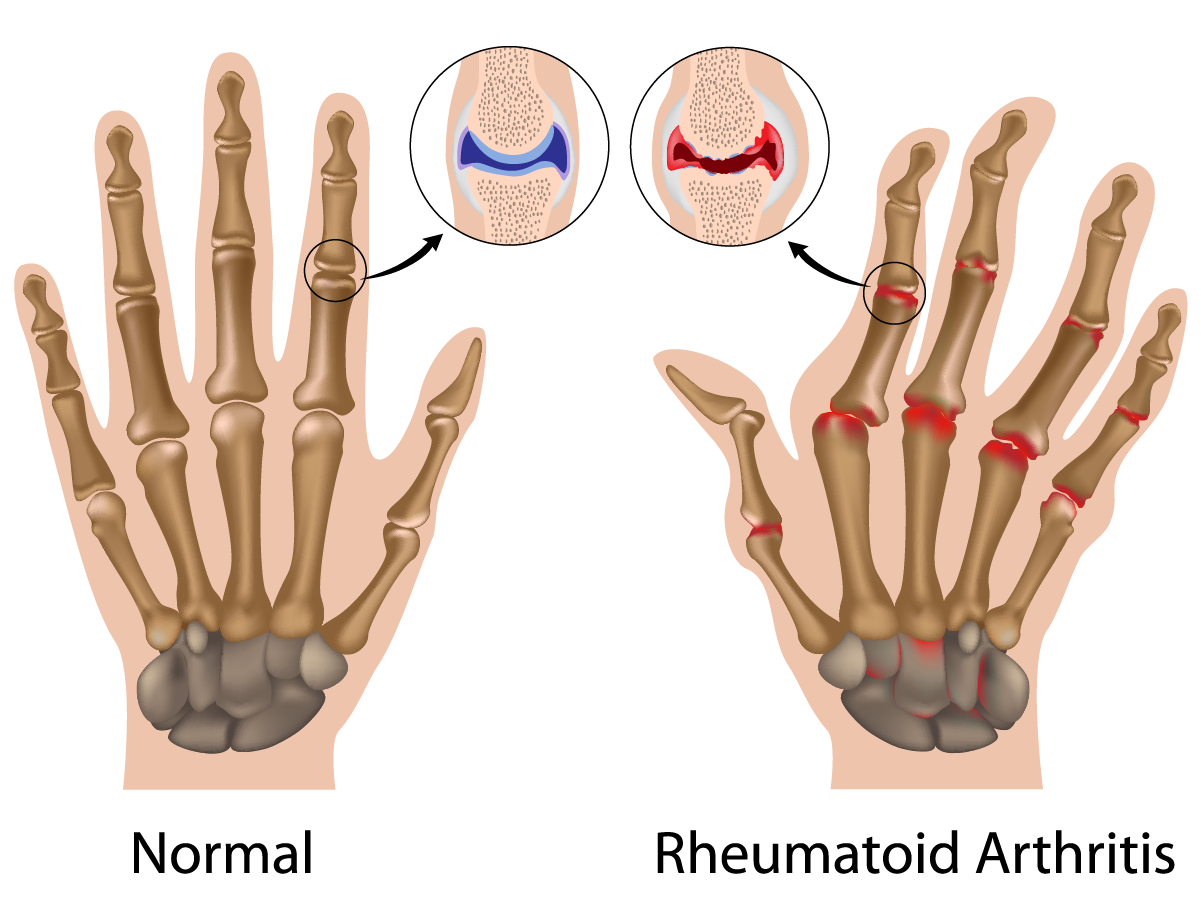
L’arthrite rhumatoïde
L’arthrite rhumatoïde est une affection auto-immune, ce qui signifie que le système immunitaire attaque ses propres cellules, en particulier à l’intérieur des articulations[19]. Étant donné que des marqueurs auto-immuns comme le facteur rhumatoïde et les anticorps anti-protéines citrullinés sont présents dans le sang bien avant que l’inflammation des articulations ne se produise, certaines théories avancent que l’auto-immunité pourrait provenir du TGI ou de la muqueuse respiratoire[20]. Il a été démontré que la réponse inflammatoire disproportionnée était déclenchée par une dysbiose dans les intestins, car certaines bactéries activent des cellules immunitaires auto-réactives[21].
Le diabète sucré de type 1
Le diabète sucré de type 1 est une maladie auto-immune qui entraine la destruction des cellules bêta dans le pancréas. Cela induit une absence de sécrétion d’insuline et affecte la régulation du glucose. En général, cette maladie est contractée pendant l’enfance. Comme nous l’avons vu avec l’arthrite rhumatoïde, les bactéries intestinales sont capables d’affecter le système immunitaire. Certaines bactéries contiennent une endotoxine appellée lipopolysaccharide (LPS) qui stimule la réponse inflammatoire et compromet le fonctionnement des cellules bêta du pancréas[22]. Certaines études ont montré que chez les personnes atteintes d’un diabète de type 1, les quantités de LPS en circulation sont plus importantes que chez les personnes non-diabétiques[23]. Les LPS peuvent également porter atteinte à la muqueuse intestinale, ce qui provoque encore plus d’inflammation et renforce l’exposition à des antigènes environnementaux. Cela provoque ensuite l’activation du système immunitaire alors qu’il est déjà réactif[24]. Dans le diabète de type 1, la diversité et la stabilité intestinales sont réduites, en comparaison avec des personnes non-diabétiques[25]. Selon certaines hypothèses, cette faible diversité pourrait limiter la capacité à digérer des aliments variés, ce qui contribue à réduire encore plus le microbiote et entraine le développement de maladies [26].
Une approche naturopathique pour la dysbiose intestinale
Les probiotiques
En ce qui concerne les maladies précédemment mentionnées, les probiotiques constituent un choix de thérapie approprié pour atténuer les symptômes liés à la dysbiose. Toutefois, avant de prendre des probiotiques, il est important de consulter un professionnel de la santé comme un médecin naturopathe, car tous les probiotiques ne fonctionnent pas de la même façon.
Dans le traitement de la colite ulcéreuse, les probiotiques traditionnels jouent un rôle limité, mais la souche E. coli Nissle spécifique et la combinaison probiotique VSL#3 ont démontré leur efficacité pour maintenir la rémission et réduire l’inflammation[27]. Il existe également d’autres probiotiques spécifiques selon les souches avec des effets bénéfiques pour les MII, notamment F. prausnitzii qui protège les intestins, entretient la barrière intestinale et stimule l’aspect protecteur du système immunitaire[28].
Afin de réduire les effets d’une dysbiose sur la dépression, on peut utiliser des psychobiotiques, qui sont une famille de probiotiques avec des effets positifs sur la santé mentale[29]. Les psychobiotiques ont également été élargis pour inclure les prébiotiques, des fibres alimentaires solubles qui nourrissent les bactéries intestinales[30]. Dans des études utilisant des psychobiotiques comme le FOS et le BGOS (prébiotiques), une baisse du cortisol au réveil, l’hormone du stress qui constitue un marqueur d’anxiété et de dépression, a été observée chez les participants[31]. D’autre part, des souches spécifiques comme Bifidobacterium longum, ont fait diminuer le cortisol matinal ainsi que les niveaux subjectifs d’anxiété et ont également renforcé le fonctionnement cognitif [32].
Les probiotiques ont un excellent profil d’innocuité pour les arthrites rhumatoïdes[33]. Leurs effets sur la réduction de certaines cytokines proinflammatoires du système immunitaire comme IL‑6 sont avérés, mais ce n’est pas le cas pour d’autres marqueurs d’inflammation ou de douleur[34]. Il semblerait que les régimes riches en probiotiques, notamment avec des aliments fermentés, des fibres alimentaires et tout un ensemble de légumes, présentent des preuves plus solides que les probiotiques pris sous la forme de suppléments pour réduire les douleurs[35]. Des preuves probantes indiquent qu’une dysbiose est présente dans des maladies auto-immunes comme l’arthrite rhumatoïde et que les probiotiques aident à rétablir le bon fonctionnement de la barrière muqueuse et à réduire l’impact des bactéries nocives[36]. Cependant, les maladies auto-immunes sont multifactorielles et d’autres aspects de ces maladies doivent être abordés. En combinaison avec d’autres ajustements, par exemple sur le mode de vie, l’alimentation, par des plantes médicinales ou la régulation des hormones, les probiotiques peuvent participer à la réussite du traitement.
Comme pour d’autres maladies auto-immunes, la barrière muqueuse des personnes souffrant de diabète sucré de type 1 est compromise[37]. La recherche de probiotiques spécifiques selon les souches ou multisouches pour traiter le diabète est limitée ; néanmoins, les probiotiques peuvent restaurer la barrière intestinale ainsi que l’équilibre bactérien. Les facteurs alimentaires comme les prébiotiques et les glucides complexes sont fermentés par les bactéries intestinales pour produire un acide gras à courte chaîne nommé le butyrate[38]. Le butyrate aide à maintenir l’intégrité intestinale, réduit la perméabilité des intestins et est anti-inflammatoire, ce qui est particulièrement important pour traiter des affections auto-immunes[39]. Par ailleurs, certaines preuves suggèrent qu’un régime sans gluten pourrait être indiqué[40]. La maladie cœliaque, une autre affection auto-immune qui implique la création d’autoanticorps contre le gluten, a été associée à d’autres maladies auto-immunes[41]. Un régime sans gluten pour les personnes atteintes de diabète de type 1 peut réduire le fardeau qui pèse sur le système immunitaire et peut en théorie prévenir le déclenchement de la maladie cœliaque[42].
