Related Articles
- 10 Déc 16
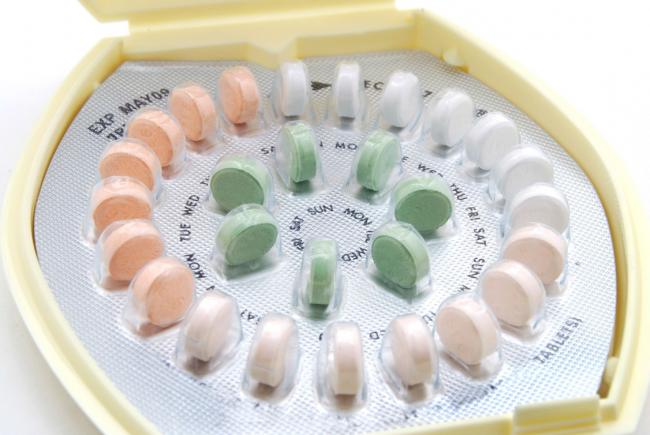
 Cet article constitue la suite, et la fin, d’un précédent texte traitant des alternatives à la pilule contraceptive. La première partie a permis d’explorer les dispositifs intra-utérins (DIU) hormonaux et cuivreux. Cette suite couvrira d’autres alternatives telles : l’anneau, le patch, le diaphragme, les préservatifs ainsi que la méthode de sensibilisation à la fertilité.
Cet article constitue la suite, et la fin, d’un précédent texte traitant des alternatives à la pilule contraceptive. La première partie a permis d’explorer les dispositifs intra-utérins (DIU) hormonaux et cuivreux. Cette suite couvrira d’autres alternatives telles : l’anneau, le patch, le diaphragme, les préservatifs ainsi que la méthode de sensibilisation à la fertilité.
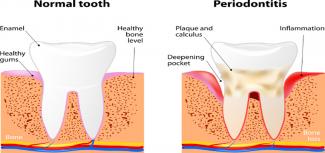
- 21 Mai 18Vous savez, bien sûr, que le nettoyage des dents est bon pour l’hygiène buccale, mais savez-vous qu’il peut aussi améliorer le bien-être de tout l’organisme ? Le brossage et le passage du fil dentaire chaque jour sont indispensables à l’entretien de nos dents et de nos gencives, mais sont peut-être encore plus importants pour la femme enceinte et pour celle qui veut l’être.
- 16 Mai 17
 L’accouchement est l’un des processus les plus bouleversants qu’une femme peut éprouver – mais si l’intensité de cet événement reste constante quelle que soit l’époque, les conditions et les attentes qui le concernent ont évolué. Dans la culture occidentale actuelle, la première fois qu’une femme est confrontée à une naissance, il s’agit généralement de celle de son propre enfant.
L’accouchement est l’un des processus les plus bouleversants qu’une femme peut éprouver – mais si l’intensité de cet événement reste constante quelle que soit l’époque, les conditions et les attentes qui le concernent ont évolué. Dans la culture occidentale actuelle, la première fois qu’une femme est confrontée à une naissance, il s’agit généralement de celle de son propre enfant. - 18 Mai 16Une maternité épanouie peut être une expérience passionnante et merveilleuse. MAIS que faire si, en place de joie et de bonheur, la future maman n’éprouve que peine et irritation et passe son temps à pleurer sans comprendre pourquoi ?
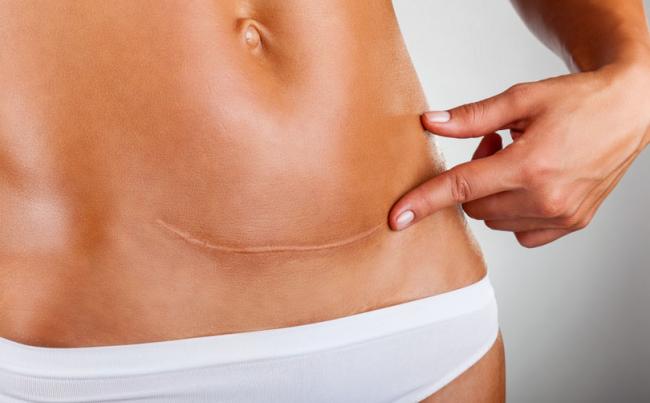
- 18 Mai 16Qu’elle soit naturelle, déclenchée, ou par césarienne, la naissance d’un enfant peut être une expérience passionnante, effrayante et difficile – alors que la vie commence à peine ! Si certains accouchements se déroulent exactement comme prévu, d’autres se révèlent plus délicats, et il est heureux que des interventions telles que l’accouchement par césarienne existent pour éviter à certaines femmes les conséquences négatives d’un accouchement problématique.
- 10 Mars 14
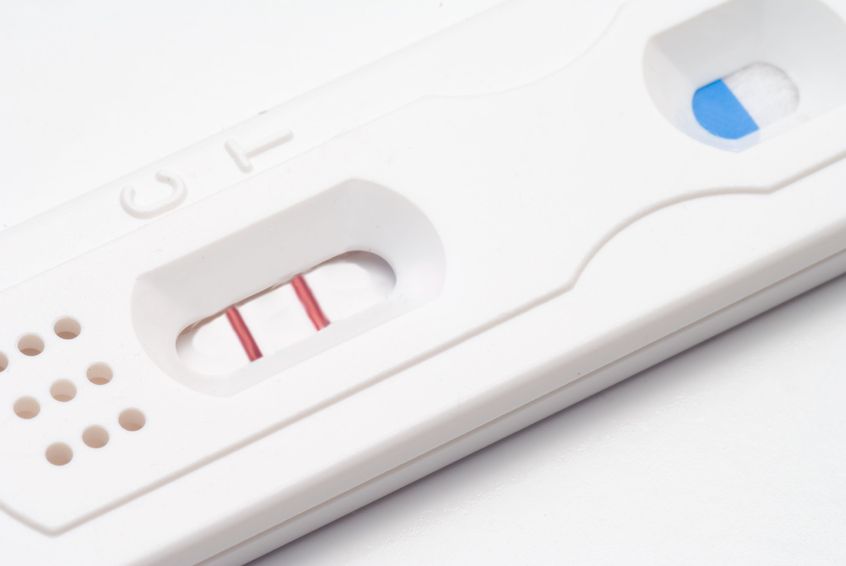
 Le nombre de couples vivant l’infertilité et/ou ayant recours à la technologie de reproduction assistée ne cesse de croitre. (1) Une étude publiée en 2012 stipulait que parmi les couples canadiens (dont la femme est âgée entre 18 et 44 ans), la prévalence d’infertilité se situait entre 11 et 15%, ce qui représente une augmentation par rapport aux données statistiques antérieures.
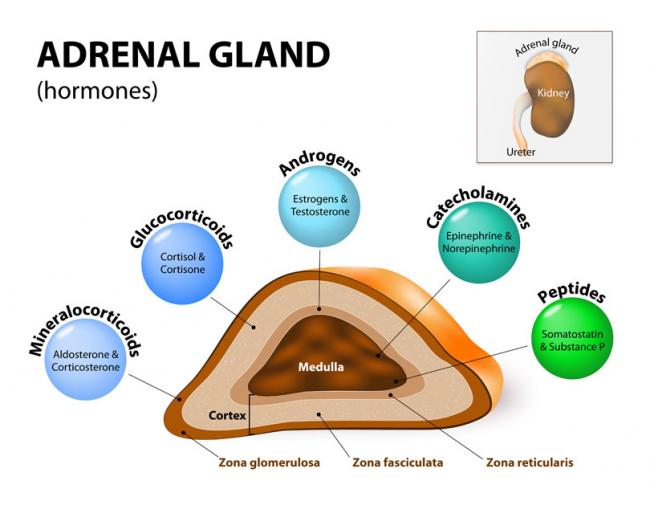
15 Déc 1618 Mai 16Un excès de stress ? On entend souvent dire aujourd’hui que nos glandes surrénales seraient trop sollicitées et fonctionneraient mal. On attribue généralement cela à des facteurs externes tels qu’une surcharge de travail, des troubles émotionnels, des problèmes relationnels ou encore des contraintes financières. Vous êtes-vous déjà dit que ça pouvait venir de causes génétiques ?16 juin 17
Le nombre de couples vivant l’infertilité et/ou ayant recours à la technologie de reproduction assistée ne cesse de croitre. (1) Une étude publiée en 2012 stipulait que parmi les couples canadiens (dont la femme est âgée entre 18 et 44 ans), la prévalence d’infertilité se situait entre 11 et 15%, ce qui représente une augmentation par rapport aux données statistiques antérieures.
15 Déc 1618 Mai 16Un excès de stress ? On entend souvent dire aujourd’hui que nos glandes surrénales seraient trop sollicitées et fonctionneraient mal. On attribue généralement cela à des facteurs externes tels qu’une surcharge de travail, des troubles émotionnels, des problèmes relationnels ou encore des contraintes financières. Vous êtes-vous déjà dit que ça pouvait venir de causes génétiques ?16 juin 17 Comprendre votre cycle menstruel ne se limite pas à estimer votre prochaine période. Connaître votre corps et faire le suivi de vos cycles menstruels peut donner une idée de votre santé hormonale et reproductive. Vous pourriez avoir des symptômes que nous considérons habituellement comme "normaux", alors que nous devrions plutôt les considérer comme "courants". 10 juil 17
Comprendre votre cycle menstruel ne se limite pas à estimer votre prochaine période. Connaître votre corps et faire le suivi de vos cycles menstruels peut donner une idée de votre santé hormonale et reproductive. Vous pourriez avoir des symptômes que nous considérons habituellement comme "normaux", alors que nous devrions plutôt les considérer comme "courants". 10 juil 17 Quand nous entendons le mot "infertilité", nous pensons souvent immédiatement à une femme qui veut tomber enceinte. Nous pensons peut-être moins souvent à la possibilité d'un problème de fertilité masculine, empêchant un couple de concevoir. Les problèmes de fertilité concernent pourtant aussi bien les hommes que les femmes. Dans cet article, nous allons explorer les informations basées sur des données probantes qui associent les expositions environnementales, l'alimentation et la supplémentation, à la fertilité et la reproduction masculine.05 Oct 1616 Avr 17
Quand nous entendons le mot "infertilité", nous pensons souvent immédiatement à une femme qui veut tomber enceinte. Nous pensons peut-être moins souvent à la possibilité d'un problème de fertilité masculine, empêchant un couple de concevoir. Les problèmes de fertilité concernent pourtant aussi bien les hommes que les femmes. Dans cet article, nous allons explorer les informations basées sur des données probantes qui associent les expositions environnementales, l'alimentation et la supplémentation, à la fertilité et la reproduction masculine.05 Oct 1616 Avr 17 Les problèmes de fertilité posés par le vieillissement maternel sont de plus en plus préoccupants pour les femmes qui souhaitent concevoir. On sait généralement que la qualité et la quantité des ovules diminuent avec l’âge, et il faut également noter que ce déclin relatif à l’âge n’est pas lié à la permanence du cycle d’ovulation et/ou de la menstruation.30 Janv 16La dysfonction érectile (DE), ou impuissance sexuelle, est le plus répandu des troubles sexuels. Environ un homme sur dix dans le monde est atteint de DE, avec une prévalence allant de 10 à 71% pour les hommes de plus de 70 ans. Si la fourchette est aussi large, c’est qu’on ne dispose pas de chiffres fiables de la fréquence ni de la prévalence de la DE – parce que la plupart des hommes ne cherchent pas de traitement. La stigmatisation sociale est trop familière, elle est toujours une réalité pour les hommes souffrant de dysfonction érectile et constitue un obstacle majeur à leur quête de soins.27 juin 14La grossesse peut être un des moments les plus palpitants de la vie d'une femme. Elle peut aussi être un des moments les plus stressants, surtout si la grossesse est compliquée par des problèmes de santé. La grossesse a beaucoup d'"effets secondaires" courants et familiers, comme la nausée, les brûlures d'estomac et la fatigue. Mais il y a aussi des problèmes plus graves susceptibles d'apparaître après la grossesse, et les symptômes ne devraient pas être négligés ou ignorés, car ce sont des signes potentiels d'une maladie qui pourrait affecter la santé à long terme.17 Août 1613 Avr 15
Les problèmes de fertilité posés par le vieillissement maternel sont de plus en plus préoccupants pour les femmes qui souhaitent concevoir. On sait généralement que la qualité et la quantité des ovules diminuent avec l’âge, et il faut également noter que ce déclin relatif à l’âge n’est pas lié à la permanence du cycle d’ovulation et/ou de la menstruation.30 Janv 16La dysfonction érectile (DE), ou impuissance sexuelle, est le plus répandu des troubles sexuels. Environ un homme sur dix dans le monde est atteint de DE, avec une prévalence allant de 10 à 71% pour les hommes de plus de 70 ans. Si la fourchette est aussi large, c’est qu’on ne dispose pas de chiffres fiables de la fréquence ni de la prévalence de la DE – parce que la plupart des hommes ne cherchent pas de traitement. La stigmatisation sociale est trop familière, elle est toujours une réalité pour les hommes souffrant de dysfonction érectile et constitue un obstacle majeur à leur quête de soins.27 juin 14La grossesse peut être un des moments les plus palpitants de la vie d'une femme. Elle peut aussi être un des moments les plus stressants, surtout si la grossesse est compliquée par des problèmes de santé. La grossesse a beaucoup d'"effets secondaires" courants et familiers, comme la nausée, les brûlures d'estomac et la fatigue. Mais il y a aussi des problèmes plus graves susceptibles d'apparaître après la grossesse, et les symptômes ne devraient pas être négligés ou ignorés, car ce sont des signes potentiels d'une maladie qui pourrait affecter la santé à long terme.17 Août 1613 Avr 15 La pré-éclampsie est une condition potentiellement mortelle qui se manifeste après vingt semaines de grossesse, donc au troisième trimestre.(1) Deux sous-types existent : la pré-éclampsie précoce qui a lieu avant la trente-quatrième semaine de grossesse et la pré-éclampsie tardive qui se manifeste après la trente-quatrième semaine .02 Sept 1623 Août 15La stérilité masculine est l’objet d’un intérêt nouveau et croissant, en lien avec la tendance à la baisse des naissances depuis une décennie. Nous vivons une époque où les familles ont moins d’enfants, plus tardivement, et souvent en faisant face à des difficultés de conception. La stérilité est un handicap à la fois physique, psychologique, financier et économique pour les individus, le système de santé et la société en général. Dans le passé, la stérilité féminine a davantage attiré l’attention, mais les données statistiques récentes et alarmantes concernant les hommes ne peuvent plus être ignorées : il faut savoir en effet que 40% de la stérilité leur est attribuée (1).23 Févr 15Le diabète gestationnel (DG) est une complication de la grossesse définie par une dégradation de la régulation glycémique qui disparait après l’accouchement. Bien que la prévalence soit variable, une récente étude des CDC indique que pas moins de 9,2% des grossesses sont concernées par le diabète gestationnel (1). Ses symptômes sont similaires à ceux du diabète de type 2 et comprennent polydipsie (soif excessive), polyurie (excès d’urine), faim et fatigue (2). La plus grande partie des cas de diabète gestationnel est diagnostiquée lors de l’examen prénatal habituel réalisé entre les 24e et 28e semaines de grossesse (2). Bien qu’elles ne répondent pas aux critères diagnostiques du DG, certaines formes plus légères d’intolérance au glucose doivent aussi être identifiées, dans la mesure où elles peuvent présenter des risques similaires.29 Janv 16Le syndrome des ovaires polykystiques (SOPK) est la cause la plus fréquente d’infertilité anovulatoire, qui touche 5 à 10% des femmes en âge de procréer. L’anovulation caractérise une activité ovarienne anormale dans laquelle les ovaires sont dans l’incapacité de produire un ovocyte (œuf) au cours du cycle menstruel. L’échographie révèle la présence de kystes multiples sur les ovaires, et l’analyse biochimique montre un déséquilibre hormonal. Un excès d’androgènes (l’hormone sexuelle masculine), causé par un taux élevé de testostérone, est mis en évidence.
La pré-éclampsie est une condition potentiellement mortelle qui se manifeste après vingt semaines de grossesse, donc au troisième trimestre.(1) Deux sous-types existent : la pré-éclampsie précoce qui a lieu avant la trente-quatrième semaine de grossesse et la pré-éclampsie tardive qui se manifeste après la trente-quatrième semaine .02 Sept 1623 Août 15La stérilité masculine est l’objet d’un intérêt nouveau et croissant, en lien avec la tendance à la baisse des naissances depuis une décennie. Nous vivons une époque où les familles ont moins d’enfants, plus tardivement, et souvent en faisant face à des difficultés de conception. La stérilité est un handicap à la fois physique, psychologique, financier et économique pour les individus, le système de santé et la société en général. Dans le passé, la stérilité féminine a davantage attiré l’attention, mais les données statistiques récentes et alarmantes concernant les hommes ne peuvent plus être ignorées : il faut savoir en effet que 40% de la stérilité leur est attribuée (1).23 Févr 15Le diabète gestationnel (DG) est une complication de la grossesse définie par une dégradation de la régulation glycémique qui disparait après l’accouchement. Bien que la prévalence soit variable, une récente étude des CDC indique que pas moins de 9,2% des grossesses sont concernées par le diabète gestationnel (1). Ses symptômes sont similaires à ceux du diabète de type 2 et comprennent polydipsie (soif excessive), polyurie (excès d’urine), faim et fatigue (2). La plus grande partie des cas de diabète gestationnel est diagnostiquée lors de l’examen prénatal habituel réalisé entre les 24e et 28e semaines de grossesse (2). Bien qu’elles ne répondent pas aux critères diagnostiques du DG, certaines formes plus légères d’intolérance au glucose doivent aussi être identifiées, dans la mesure où elles peuvent présenter des risques similaires.29 Janv 16Le syndrome des ovaires polykystiques (SOPK) est la cause la plus fréquente d’infertilité anovulatoire, qui touche 5 à 10% des femmes en âge de procréer. L’anovulation caractérise une activité ovarienne anormale dans laquelle les ovaires sont dans l’incapacité de produire un ovocyte (œuf) au cours du cycle menstruel. L’échographie révèle la présence de kystes multiples sur les ovaires, et l’analyse biochimique montre un déséquilibre hormonal. Un excès d’androgènes (l’hormone sexuelle masculine), causé par un taux élevé de testostérone, est mis en évidence.
Actualités
Votre abonnement n'a pas pu être enregistré. Veuillez réessayer.
Vous vous êtes abonné avec succès à l’infolettre de Naturopathic Currents.
Les plus populaires
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13