Related Articles
- 01 Ott 13
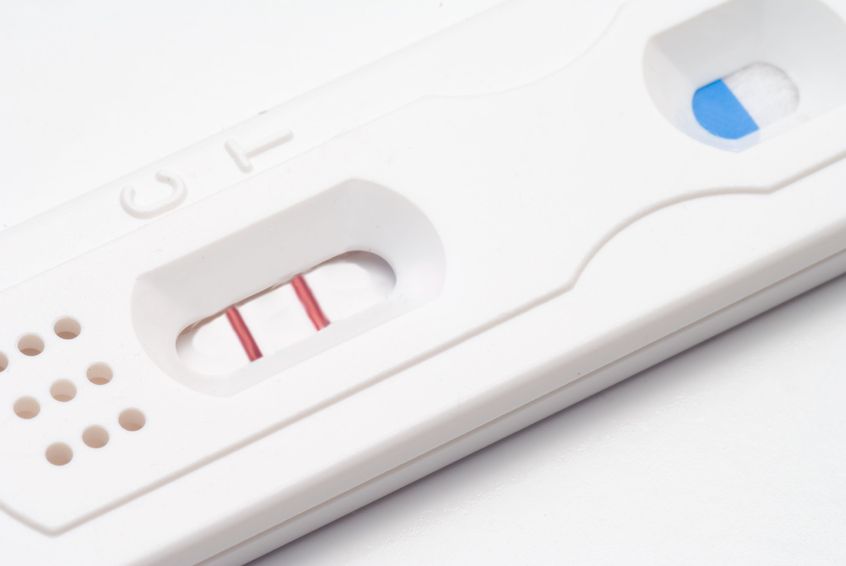
 Mentre una gravidanza è una bella notizia, soprattutto per le coppie che hanno affrontato sfide della fertilità, è solo l'inizio di un cammino. Purtroppo non tutte le gravidanze sono 40 settimane di gestazione tranquilla. Alcune donne si trovano ad affrontare problemi più gravi, come il sanguinamento vaginale (e i conseguenza presunti una minacce d'aborto) dando origine a molto stress ed ansia, mentre altri soffrono di nausea e vomito
Mentre una gravidanza è una bella notizia, soprattutto per le coppie che hanno affrontato sfide della fertilità, è solo l'inizio di un cammino. Purtroppo non tutte le gravidanze sono 40 settimane di gestazione tranquilla. Alcune donne si trovano ad affrontare problemi più gravi, come il sanguinamento vaginale (e i conseguenza presunti una minacce d'aborto) dando origine a molto stress ed ansia, mentre altri soffrono di nausea e vomito - 26 Ago 13
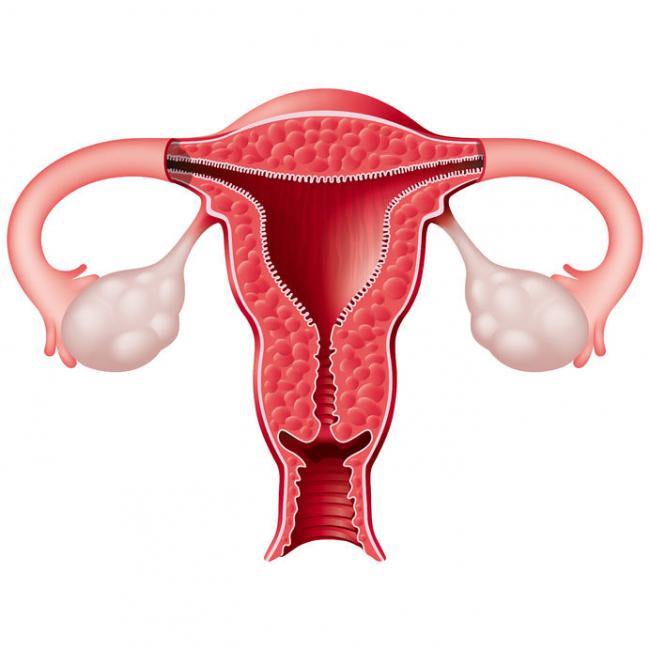
 I problemi mestruali, sono preoccupazioni comuni nella salute della donna, in particolare la sindrome premestruale (SPM), le mestruazioni dolorose (dismenorrea), e l’irregolarità o l’assenza del ciclo mestruale (amenorrea). Questi sintomi possono procurare, per il protrarsi di alcune condizioni mediche la sindrome dell'ovaio policistico (PCOS), l’endometriosi e dei fibromi uterini. Sebbene non sono mortali, questi problemi hanno ripercussioni negative sulla qualità della vita della donna ed sono un segnale di problemi irrisolti.
I problemi mestruali, sono preoccupazioni comuni nella salute della donna, in particolare la sindrome premestruale (SPM), le mestruazioni dolorose (dismenorrea), e l’irregolarità o l’assenza del ciclo mestruale (amenorrea). Questi sintomi possono procurare, per il protrarsi di alcune condizioni mediche la sindrome dell'ovaio policistico (PCOS), l’endometriosi e dei fibromi uterini. Sebbene non sono mortali, questi problemi hanno ripercussioni negative sulla qualità della vita della donna ed sono un segnale di problemi irrisolti. - 26 Ago 13
 Un area emergente di studio, si dedica allo studio dell'impatto di alcuni fattori nei primi anni di vita includendo l’impatto dell’alimentazione sullo sviluppo delle malattie in seguito nella vita. Il fetal origins of adult disease (FOAD-SPIRIT) è un campo il cui obbiettivo è quello di studiare il legame tra condizioni materno/ fetale durante vita prenatale, e il rischio di malattia cronica nell'età adulta. Anche se questo potrebbe sembrare scontato, l'estensione della sua influenza non fu realizzato fino a poco tempo fa.
Un area emergente di studio, si dedica allo studio dell'impatto di alcuni fattori nei primi anni di vita includendo l’impatto dell’alimentazione sullo sviluppo delle malattie in seguito nella vita. Il fetal origins of adult disease (FOAD-SPIRIT) è un campo il cui obbiettivo è quello di studiare il legame tra condizioni materno/ fetale durante vita prenatale, e il rischio di malattia cronica nell'età adulta. Anche se questo potrebbe sembrare scontato, l'estensione della sua influenza non fu realizzato fino a poco tempo fa. - 20 Dic 16
 L’anello e il cerotto sono due varianti della pillola anticoncezionale per via orale e quindi hanno lo stesso rischio, medesimi effetti collaterali e controindicazioni della “pillola”. Prodotti come Nuvaring ed Evrapatch rilasciano ormoni femminili (sia estrogeni che progestina) per tre settimane per bloccare l’ovulazione e prevenire una gravidanza.
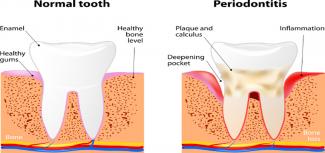
L’anello e il cerotto sono due varianti della pillola anticoncezionale per via orale e quindi hanno lo stesso rischio, medesimi effetti collaterali e controindicazioni della “pillola”. Prodotti come Nuvaring ed Evrapatch rilasciano ormoni femminili (sia estrogeni che progestina) per tre settimane per bloccare l’ovulazione e prevenire una gravidanza. - 31 Mag 18Certo, la pulizia dentale è ottima per la nostra salute orale, ma sapevi che può anche migliorare il benessere di tutto il corpo?
- 05 Gen 16La Sindrome dell’ovaio policistico (PCOS) è la causa più frequente di infertilità anovulatoria pari al 5-10% delle donne in età fertile. L’Anovulazione è l’anormale funzione ovarica che impedisce alle ovaie il rilascio di ovocita (uova) durante il ciclo mestruale (1, 2). In PCOS, è stata rilevata mediante l’utilizzo di ultrasuoni una frequente formazione di cisti ovariche e di un chiaro squilibrio ormonale conseguenzialmente confermato da risultati biochimici. In una patologia di PCOS si evidenzia una quantità eccessiva di androgeni (gli ormoni sessuali maschili) risultante da livelli elevati di testosterone (2). L'eccesso di testosterone manifesta chiaramente alcuni dei segni e sintomi della PCOS come l’irsutismo con una presenza eccessiva di peluria sul viso e sul corpo, acne e diradamento o caduta dei capelli. (2,3).
- 06 Mag 16La gioia della maternità può essere una meravigliosa esperienza. Ma, che cosa succede se invece di essere felice, laneo mamma, vivendo questa bellissima esperienza, si sente inspiegabilmente irritabile e piange spesso? Che cosa succede se invece di provare trasporto nel guardare il suo bambino, si sente infelice e teme di potergli fare del male? E che cosa succede se invece di essere felice, lei pensa al suicidio? Aggiungi a questo, un senso di vergogna, di confusione e la paura di credere di vivere completamente da sola questa esperienza. Questa è una realtà che riguarda circa il 13% delle donne che partoriscono (1).
- 05 Ott 16
 Il caffè fa parte della vostra routine quotidiana? Siete convinti che vi faccia bene? Avete mai pensato che potrebbe non essere così? Tutto con la dovuta moderazione, giusto? Da quando sono esplosi i fenomeni Starbucks, Tim Horton e Second Cup, la popolarità della caffeina ha portato la gente a chiudere un occhio sui suoi effetti negativi per la salute. Ora il pericolo è chiaro ed è difficile negare che ci siano molti sintomi generati da questa sostanza che crea dipendenza.
Il caffè fa parte della vostra routine quotidiana? Siete convinti che vi faccia bene? Avete mai pensato che potrebbe non essere così? Tutto con la dovuta moderazione, giusto? Da quando sono esplosi i fenomeni Starbucks, Tim Horton e Second Cup, la popolarità della caffeina ha portato la gente a chiudere un occhio sui suoi effetti negativi per la salute. Ora il pericolo è chiaro ed è difficile negare che ci siano molti sintomi generati da questa sostanza che crea dipendenza. - 03 Mar 14
 Il numero di coppie che ha problemi di infertilità e/o ricorre alle tecnologie di riproduzione assistita (PMA, chiamate anche ART, dall'inglese Assisted Reproductive Technology) è in aumento (1). Uno studio pubblicato nel 2012 ha rilevato che tra le coppie canadesi (con donne tra i 18 e i 40) la prevalenza di infertilità variava tra l'11% e il 15%, il che rappresentava un aumento rispetto alle statistiche precedenti
Il numero di coppie che ha problemi di infertilità e/o ricorre alle tecnologie di riproduzione assistita (PMA, chiamate anche ART, dall'inglese Assisted Reproductive Technology) è in aumento (1). Uno studio pubblicato nel 2012 ha rilevato che tra le coppie canadesi (con donne tra i 18 e i 40) la prevalenza di infertilità variava tra l'11% e il 15%, il che rappresentava un aumento rispetto alle statistiche precedenti - 23 Dic 16
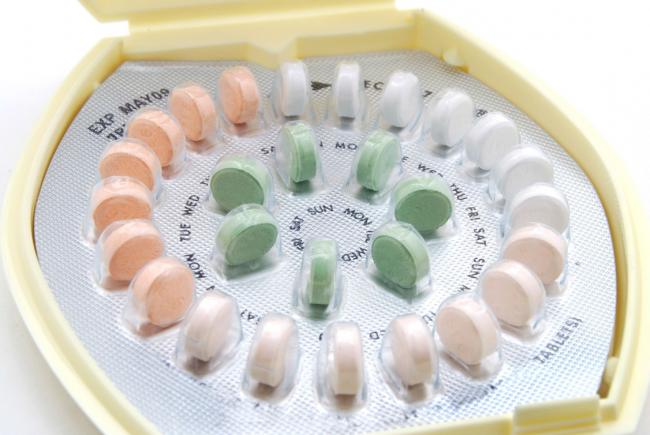
 Il composto della pillola anticoncezionale ad assunzione orale è generalmente una combinazione di estrogeni e progestina da assumersi oralmente per prevenire la fertilità femminile e la gravidanza. È stata introdotta per la prima volta nel 1960 e da allora ha subito molte modifiche ed è stata usata da milioni di donne in tutto il mondo. Delle donne canadesi che utilizzano metodi contraccettivi, il 32% usa la pillola come metodo di contraccezione
Il composto della pillola anticoncezionale ad assunzione orale è generalmente una combinazione di estrogeni e progestina da assumersi oralmente per prevenire la fertilità femminile e la gravidanza. È stata introdotta per la prima volta nel 1960 e da allora ha subito molte modifiche ed è stata usata da milioni di donne in tutto il mondo. Delle donne canadesi che utilizzano metodi contraccettivi, il 32% usa la pillola come metodo di contraccezione - 30 Apr 17La fertilità risente dei relativi processi di invecchiamento biologico femminile e rappresenta una sempre crescente preoccupazione per coloro che desiderano concepire. È comunemente noto che la qualità e quantità dell’ovulo femminile subisce un calo con l’avanzare dell’età; ed è inoltre importante essere consapevoli del fatto che questo declino legato all’età avviene indipendentemente dai continui cicli ovulatori e/o dalle mestruazioni [1].
- 05 Gen 16Tra tutte le disfunzioni sessuali, la disfunzione erettile (DE) è la più frequente (1). Circa 1 uomo su 10 in tutto il mondo ne soffre, con una percentuale compresa tra il 10 e il 71% degli uomini di età superiore a 70 anni (2). L’incidenza e la prevalenza di questo disturbo rientrano in una sfera talmente ampia da non disporre di cifre attendibili, anche perché la maggior parte degli uomini non ricorre ad alcun trattamento. Lo stigma sociale è fin troppo diffuso e continua a rappresentare la vera difficoltà per molti uomini di curare questo disturbo, rappresentando il più grande ostacolo a ricorrere alle relative cure. Correlata ai primi segni di una malattia cardiovascolare, tale disfunzione rappresenta grande preoccupazione perché sono giovani il 25% degli uomini che ne soffre (sotto i 40 anni di età) (3).
- 31 Lug 17Spesso, quando sentiamo la parola "sterilità", la nostra mente va immediatamente a una donna che vuole partorire un bambino. Meno spesso, forse, ci capita subito di pensare al potenziale che un problema riproduttivo maschile potrebbe essere la ragione per cui una coppia sta avendo problemi a concepire.
- 31 Mag 17Ci sono molte controversie nelle cure sanitarie, per quanto riguarda la corretta quantità di proteine nella dieta, necessaria per una salute ottimale.
- 02 Giu 14
 La gravidanza può essere una delle esperienze più emozionanti della vita di una donna. Tuttavia, essa può anche essere uno dei momenti più stressanti, soprattutto se ci sono complicazioni dovute a questioni di salute. Sono molti gli "effetti collaterali" comuni della gravidanza, come ad esempio nausea, bruciore di stomaco e stanchezza. 04 Ago 15Vi è un nuovo e crescente interesse verso l’infertilità maschile, considerate le recenti tendenze che negli ultimi dieci anni hanno soppiantato una vecchia concezione. I tempi indicano la presenza di famiglie con meno prole, avuti in età più adulta e spesso con maggiori difficoltà a procreare. L‘infertilità rappresenta un disturbo fisico e psicologico, finanziariamente oneroso per gli individui, il sistema sanitario e la società. Storicamente, il maggiore interesse è rivolto all’infertilità femminile, in ogni caso, più recentemente non si possono ignorare le allarmanti statistiche sull’infertilità maschile. Per esempio, il 40% di infertilità è maschile (1).08 Giu 15
La gravidanza può essere una delle esperienze più emozionanti della vita di una donna. Tuttavia, essa può anche essere uno dei momenti più stressanti, soprattutto se ci sono complicazioni dovute a questioni di salute. Sono molti gli "effetti collaterali" comuni della gravidanza, come ad esempio nausea, bruciore di stomaco e stanchezza. 04 Ago 15Vi è un nuovo e crescente interesse verso l’infertilità maschile, considerate le recenti tendenze che negli ultimi dieci anni hanno soppiantato una vecchia concezione. I tempi indicano la presenza di famiglie con meno prole, avuti in età più adulta e spesso con maggiori difficoltà a procreare. L‘infertilità rappresenta un disturbo fisico e psicologico, finanziariamente oneroso per gli individui, il sistema sanitario e la società. Storicamente, il maggiore interesse è rivolto all’infertilità femminile, in ogni caso, più recentemente non si possono ignorare le allarmanti statistiche sull’infertilità maschile. Per esempio, il 40% di infertilità è maschile (1).08 Giu 15 La fertilità maschile si misura in base alla qualità dello sperma e alla conta degli spermatozoi. Un uomo viene considerato a rischio di infertilità se la sua conta spermatica è inferiore ai 20 milioni per ml, e può essere sterile se la conta è inferiore ai 500.000 per ml. L’analisi del liquido seminale viene solitamente effettuata tramite microscopio ottico e microscopio elettronico a scansione.02 Set 16
La fertilità maschile si misura in base alla qualità dello sperma e alla conta degli spermatozoi. Un uomo viene considerato a rischio di infertilità se la sua conta spermatica è inferiore ai 20 milioni per ml, e può essere sterile se la conta è inferiore ai 500.000 per ml. L’analisi del liquido seminale viene solitamente effettuata tramite microscopio ottico e microscopio elettronico a scansione.02 Set 16 Ci sono pochi dubbi che il vostro medico di famiglia creda fermamente nell’ “assistenza sanitaria al pre-concepimento”, vale a dire la cura e il counseling designati per aiutare voi e il vostro partner ad essere più in salute possibile prima di concepire vostro figlio. In effetti l’assistenza al pre-concepimento è considerata dai medici e dalle autorità in materia di salute generale come molto importante per la fertilità, per i risultati della gravidanza e potenzialmente per la salute futura di vostro figlio quando sarà adulto. 05 Ott 15Lo facciamo tutti. Sai di esserne colpevole anche tu. Vuoi sapere di cosa sto parlando? Igiene personale. Non fraintendetemi. Questo articolo non vuole parlare dell’igiene personale come di un qualcosa di cui vergognarsi perché legato ai lavaggi dei capelli o dei denti. Quello che si vuole evidenziare è la consapevolezza di come la maggior parte dei prodotti per la pulizia e la cura personale potrebbero essere di fatto dannosi per la nostra salute. L’equivoco maggiore in cui incorrere è ritenere che un prodotto esposto e acquistabile possa ritenersi sicuro, vero? e che se un prodotto è esposto e acquistabile, è sicuro, giusto? Sbagliato. La maggior parte dei prodotti sul mercato per la cura personale (PCP) contengono tossine incidenti sugli ormoni e causa di alcune gravi malattie.30 Giu 17Capire il ciclo mestruale comporta più di una semplice stima sul tuo prossimo ciclo. Conoscere il proprio corpo e monitorare i propri cicli mestruali può fornire la comprensione della tua salute ormonale e riproduttiva. Potresti avvertire dei sintomi che noi di solito etichettiamo come "normali", quando dovremmo invece chiamarli "comuni". Questi sintomi potrebbero essere segni di: uno squilibrio ormonale, una carenza di nutrienti, troppo bassa o troppo alta percentuale di grasso corporeo (1), o il risultato dello stress.
Ci sono pochi dubbi che il vostro medico di famiglia creda fermamente nell’ “assistenza sanitaria al pre-concepimento”, vale a dire la cura e il counseling designati per aiutare voi e il vostro partner ad essere più in salute possibile prima di concepire vostro figlio. In effetti l’assistenza al pre-concepimento è considerata dai medici e dalle autorità in materia di salute generale come molto importante per la fertilità, per i risultati della gravidanza e potenzialmente per la salute futura di vostro figlio quando sarà adulto. 05 Ott 15Lo facciamo tutti. Sai di esserne colpevole anche tu. Vuoi sapere di cosa sto parlando? Igiene personale. Non fraintendetemi. Questo articolo non vuole parlare dell’igiene personale come di un qualcosa di cui vergognarsi perché legato ai lavaggi dei capelli o dei denti. Quello che si vuole evidenziare è la consapevolezza di come la maggior parte dei prodotti per la pulizia e la cura personale potrebbero essere di fatto dannosi per la nostra salute. L’equivoco maggiore in cui incorrere è ritenere che un prodotto esposto e acquistabile possa ritenersi sicuro, vero? e che se un prodotto è esposto e acquistabile, è sicuro, giusto? Sbagliato. La maggior parte dei prodotti sul mercato per la cura personale (PCP) contengono tossine incidenti sugli ormoni e causa di alcune gravi malattie.30 Giu 17Capire il ciclo mestruale comporta più di una semplice stima sul tuo prossimo ciclo. Conoscere il proprio corpo e monitorare i propri cicli mestruali può fornire la comprensione della tua salute ormonale e riproduttiva. Potresti avvertire dei sintomi che noi di solito etichettiamo come "normali", quando dovremmo invece chiamarli "comuni". Questi sintomi potrebbero essere segni di: uno squilibrio ormonale, una carenza di nutrienti, troppo bassa o troppo alta percentuale di grasso corporeo (1), o il risultato dello stress.
Newsletter
Le informazioni fornite non sono valide. Controlla il formato del campo e riprova.
La tua iscrizione è andata a buon fine.
Più Popolare
- 17 Giu 13
- 17 Giu 13
- 17 Giu 13
- 01 Lug 13
- 17 Giu 13
- 17 Giu 13
- 17 Giu 13
- 01 Lug 13
- 17 Giu 13
- 17 Giu 13
- 17 Giu 13
- 01 Lug 13