Related Articles
- 23 Avr 15La prévalence du surpoids et de l’obésité en Amérique du Nord a littéralement explosé ces dernières années, et les méthodes de contrôle du poids utilisées n’ont guère rencontré de succès. La science comme le grand public s’intéressent depuis des décennies aux moyens naturels ou artificiels pour perdre du poids, le plus récent d’entre eux étant la Garcinia cambogia (G. cambogia) et son extrait, l’acide (-)-hydroxycitrique (HCA).
- 06 Déc 18Les produits de santé naturelle permettant un contrôle vérifiable de la glycémie ont longtemps fait défaut. Le Gymnema et l’écorce de margose entraient souvent dans la composition de ces produits, bien que les preuves de leur efficacité soient, au mieux, peu nombreuses.
- 09 Mai 19L’acné est l’une des maladies cutanées chroniques les plus répandues : 80 à 90% de la population est touchée, un jour ou l’autre, par l’acné [1]. Il s’agit d’une affection relativement bénigne, qui peut pourtant avoir des effets très lourds sur la santé psychique. On observe, indépendamment de sa gravité, un taux plus élevé d’anxiété et de dépression chez les personnes qui en sont atteintes [2]. Alors même que les lésions acnéiques ont disparu, les cicatrices et traces pigmentaires qui peuvent subsister ont parfois un impact durable sur l’estime de soi et le bien-être psychologique. Ces seules raisons justifient que l’on recherche des solutions efficaces pour lutter contre l’acné.
- 17 Janv 19Nous avons tous entendu dire que la peau est l’organe le plus étendu de notre corps. Elle joue un rôle crucial pour nous protéger des agents pathogènes, pour nous aider à éliminer nos déchets organiques, réguler notre température corporelle, et communiquer des informations grâce au sens du toucher. Il s’agit d’un organe complexe, affecté par notre environnement interne et externe, et dont on ne peut parler sans parler aussi d’autres systèmes organiques.
- 30 Oct 18Vos règles sont en retard, vraiment en retard. Vous n’êtes pourtant pas enceinte, ni en phase de ménopause. Vous avez peut-être manqué un cycle, ou plusieurs. Naturellement, c’est inquiétant : la plupart des femmes dont les règles ne se décident pas à apparaitre font des tests de grossesse répétés, pour se rassurer. Mais les raisons qui peuvent expliquer l’absence des règles vont bien au-delà d’une éventuelle grossesse.
- 16 Mars 19Le déséquilibre hormonal est un problème de santé auquel beaucoup de femmes sont confrontées. Celles-ci sont amenées à prendre de plus en plus de responsabilités – elles prodiguent des soins, s’occupent des enfants, en plus de travailler pour joindre les deux bouts. Elles sont en conséquence exposées à un stress de plus en plus important, une des principales raisons de l’augmentation des déséquilibres hormonaux. L’exposition aux xéno-œstrogènes dans les produits ménagers (les emballages en plastique), dans les produits de soins, voire dans l’eau du robinet, peut contribuer aux déséquilibres hormonaux, de même que de mauvais choix alimentaires. Ces déséquilibres proviennent de changements dans les taux relatifs d’œstrogènes, de progestérone et/ou de testostérone : les œstrogènes peuvent être trop élevés par rapport à la progestérone, ou la progestérone être trop faible, faisant paraitre élevé le taux d’œstrogènes. Notre article se concentrera sur ces déséquilibres entre progestérone et œstrogènes.
- 30 Nov 18L’inflammation est devenue un sujet d’actualité pour le monde médical, faisant l’objet de recherches croissantes. On pensait naguère que l’arthrite et l’inflammation articulaire commençaient et finissaient dans les articulations, sans autres influences ni connexions. Nous savons aujourd’hui qu’une inflammation intestinale peut avoir des effets sur l’inflammation articulaire, augmenter le risque de diabète, provoquer des poussées d’eczéma, et même déclencher anxiété et dépression dans le cerveau [1]. Les choses sont donc un peu plus complexes qu’on ne le supposait, et prennent nettement plus de temps à corriger, mais le savoir c’est le pouvoir, et la prise de conscience est la première étape vers le progrès.
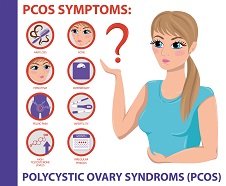
- 30 Oct 18Le syndrome des ovaires polykystiques (SOPK) est une affection qui se manifeste par des symptômes reproductifs et endocriniens, et touche à l’heure actuelle au moins 5 à 10% des femmes en âge de procréer [1].
- 20 Août 18Le jeûne est l’abstinence volontaire de nourriture et de boisson calorique pendant une période donnée. En d’autres termes, jeûner, c’est ne pas manger – c’est aussi simple que cela. Mais ne nous laissons pas abuser par cette simplicité : se priver de nourriture peut avoir des bénéfices nombreux et surprenants.
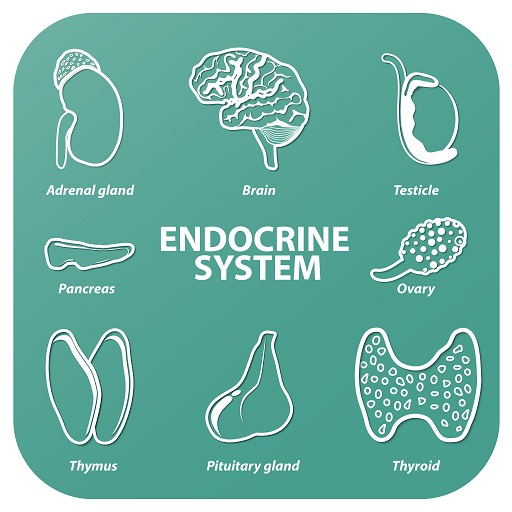
- 09 Mai 19Vous êtes-vous déjà demandé comment fait votre corps pour réguler son métabolisme, l’humeur, la température, le rythme cardiaque, ou même la fécondité ? Il faut remercier votre système endocrinien, capable de réguler toutes ces fonctions grâce à un système de glandes, des petits organes sécrétoires chargés de libérer des hormones dans l’organisme [1][2][3][4][5]. Les troubles endocriniens surviennent en cas de déséquilibre et/ou de carence d’une ou plusieurs hormones [1][2].
- 30 Nov 18Les fluctuations du taux d’hormones sexuelles au cours du cycle menstruel peuvent avoir des conséquences sur le niveau d’énergie et l’humeur, et provoquer des symptômes physiques, le plus souvent en fin de phase lutéale. Ces symptômes peuvent pourtant apparaitre dès l’ovulation et se poursuivre jusqu’aux règles, comme c’est souvent le cas dans le trouble dysphorique prémenstruel (TDPM), une affection grave et spécifique, inscrite au DSM-5 et reconnue pour ses importants symptômes cognitifs et affectifs [1].
- 09 Mai 19Commençons par la définition clinique habituelle : la dépression est un sentiment durable de tristesse, de désespoir, et une perte d’intérêt pour ses propres activités. Elle peut se manifester entre autres par des symptômes physiques tels que de la fatigue, des douleurs chroniques, des maux de tête et des problèmes digestifs. Les symptômes permettant un diagnostic doivent durer depuis au moins deux semaines et provoquer un trouble ou un affaiblissement significatifs.
- 20 Août 18La plupart des femmes passent toute leur vie à attendre la fin de leur cycle menstruel. « Finis, les ennuis ! » proclamons-nous, en supposant que cette époque bénie nous apportera la fin de tous les déséquilibres hormonaux, maux de tête, problèmes de peau, ballonnements, instabilité d’humeur – et bien sûr, risques de grossesse. Mais à mesure que le temps passe, et que de nouveaux symptômes apparaissent, la question peut devenir : « Suis-je en train de changer, ou est-ce autre chose ? », question très pertinente puisque les symptômes en cours de ménopause peuvent aller bien au-delà des traditionnelles sueurs nocturnes et bouffées de chaleur.
- 16 Avr 19On décrit généralement le syndrome des ovaires polykystiques (SOPK) comme un trouble hormonal, mais c’est aussi, et peut-être avant tout, un trouble métabolique. Les femmes atteintes du SOPK présentent souvent des symptômes de dérèglements hormonaux divers, y compris des troubles de la reproduction, qui se manifestent d’ordinaire par un allongement des règles et une ovulation irrégulière. En outre, on observe fréquemment une dérégulation à long terme du métabolisme des lipides et de l’équilibre de l’insuline et du glucose, pouvant, à terme, entrainer une stéatose hépatique non alcoolique (SHNA). Les autres symptômes courants du SOPK sont notamment l’acné (ce que j’appelle une « barbe d’acné », d’après la zone du visage et du cou où elle apparait), une croissance anormale de poils sur le visage, ainsi que des difficultés à perdre du poids, en particulier la graisse corporelle. Ces troubles apparaissent généralement lorsque le taux d’hormones androgènes, telles que la testostérone, devient trop élevé, les ovaires cessant alors de fonctionner normalement.
- 02 Sept 16
- 17 juil 16
 L’acné vulgaire représente la pathologie dermatologique la plus fréquente vue par les médecins. Cette maladie peut causer beaucoup de détresse, entraînant chez certains une baisse de l’estime de soi. Les scores de santé mentale chez les patients atteints d’acné sont plus élevés comparés à un certain nombre d’autres pathologies chroniques. Souvent, les malades utilisent des médicaments allopathiques tels que la pilule contraceptive, des stéroïdes diurétiques (Spironolactone) ou encore le rétinoïde : Accutane, spécifique à l’acné.
L’acné vulgaire représente la pathologie dermatologique la plus fréquente vue par les médecins. Cette maladie peut causer beaucoup de détresse, entraînant chez certains une baisse de l’estime de soi. Les scores de santé mentale chez les patients atteints d’acné sont plus élevés comparés à un certain nombre d’autres pathologies chroniques. Souvent, les malades utilisent des médicaments allopathiques tels que la pilule contraceptive, des stéroïdes diurétiques (Spironolactone) ou encore le rétinoïde : Accutane, spécifique à l’acné. - 18 Mai 16Une maternité épanouie peut être une expérience passionnante et merveilleuse. MAIS que faire si, en place de joie et de bonheur, la future maman n’éprouve que peine et irritation et passe son temps à pleurer sans comprendre pourquoi ?
- 06 juil 19Ma fleur est l’une des premières à s’ouvrir au printemps. Sur les pelouses soigneusement entretenues, mon jaune vif et gai se remarque très vite. Je suis partout, et tout le monde me reconnait. Je m’implante sans rien demander à personne et suis bien difficile à éliminer. Vous l’avez sans doute deviné : je suis le pissenlit, l’obstiné pissenlit.
- 10 Mars 14
 Le nombre de couples vivant l’infertilité et/ou ayant recours à la technologie de reproduction assistée ne cesse de croitre. (1) Une étude publiée en 2012 stipulait que parmi les couples canadiens (dont la femme est âgée entre 18 et 44 ans), la prévalence d’infertilité se situait entre 11 et 15%, ce qui représente une augmentation par rapport aux données statistiques antérieures.
24 Août 14Le terme dysménorrhée est couramment utilisé pour désigner des menstruations (règles) douloureuses. Considérée comme une affection parmi les plus courantes chez les femmes, le traitement efficace consiste à déterminer la cause première et à la traiter. Quand la douleur est due à une affection pelvienne ou systémique spécifique, elle est qualifiée de dysménorrhée secondaire. En l’absence de maladie ou d’anomalies physiques, la douleur menstruelle est qualifiée de dysménorrhée primaire. Le diagnostic précis repose sur un examen physique approfondi et une analyse des antécédents de santé. Une étude sur des femmes canadiennes en période de règles a révélé que 60 % souffraient de dysménorrhée primaire. 51 % ont déclaré que la douleur avait un impact sur leurs activités durant la journée et 17 % ont déclaré qu’elles ne pouvaient pas travailler (1). Les implications sociales et la prévalence de cette pathologie justifient des traitements sûrs et durables. Cet article explore les options thérapeutiques pour la dysménorrhée primaire.
Le nombre de couples vivant l’infertilité et/ou ayant recours à la technologie de reproduction assistée ne cesse de croitre. (1) Une étude publiée en 2012 stipulait que parmi les couples canadiens (dont la femme est âgée entre 18 et 44 ans), la prévalence d’infertilité se situait entre 11 et 15%, ce qui représente une augmentation par rapport aux données statistiques antérieures.
24 Août 14Le terme dysménorrhée est couramment utilisé pour désigner des menstruations (règles) douloureuses. Considérée comme une affection parmi les plus courantes chez les femmes, le traitement efficace consiste à déterminer la cause première et à la traiter. Quand la douleur est due à une affection pelvienne ou systémique spécifique, elle est qualifiée de dysménorrhée secondaire. En l’absence de maladie ou d’anomalies physiques, la douleur menstruelle est qualifiée de dysménorrhée primaire. Le diagnostic précis repose sur un examen physique approfondi et une analyse des antécédents de santé. Une étude sur des femmes canadiennes en période de règles a révélé que 60 % souffraient de dysménorrhée primaire. 51 % ont déclaré que la douleur avait un impact sur leurs activités durant la journée et 17 % ont déclaré qu’elles ne pouvaient pas travailler (1). Les implications sociales et la prévalence de cette pathologie justifient des traitements sûrs et durables. Cet article explore les options thérapeutiques pour la dysménorrhée primaire.
Actualités
Votre abonnement n'a pas pu être enregistré. Veuillez réessayer.
Vous vous êtes abonné avec succès à l’infolettre de Naturopathic Currents.
Les plus populaires
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13