Related Articles
- 12 4月 18身体は脆いもので、年齢を重ねるにつれて急性損傷や慢性変性疾患が生じやすくなります。医療には、消毒や包帯、骨折した部分を添え木で支える、杖で痛む膝を圧迫するなど、怪我に対する処置法がいくつかあります。しかし、通常、こうした基本的な処置を施す以外には、自然に治癒するのを待つしかありません。
- 12 4月 18100年前には、食品に「敏感」であるという概念は馬鹿げていると考えられていたでしょう。10年前でさえ、「グルテンフリー」や「乳製品アレルギー」という用語は珍しく、大半の人がその意味や重要性について知らずに判断していました。今日、多くの学校で、ナッツフリーの給食を提供していて、あらゆる製品成分を適切に表示するための法律が可決されました。しかし、多くの家庭において、特定の食品を避けた食事を用意するのは大変で、もし食物敏感症をお持ちなら、社交の場に参加することがどれほどストレスになるかをご存じでしょう。食物感受症はなぜ生じるのでしょう?食物が劇的に変化し、私たちはそれを認識できなくなったのでしょうか?それとも、私たちの体がより敏感になったのでしょうか?おそらくその両方があてはまりますが、ヒトゲノムは過去2000年間ほぼ変わっていないことを考えると、遺伝子が変異した可能性は低いです。
- 31 12月 17きのこは、主にその免疫システム、神経システム、肝臓、そして腎臓に対する効能により、薬として数千年もの間利用されて来ました。
- 09 7月 15
- 02 7月 14
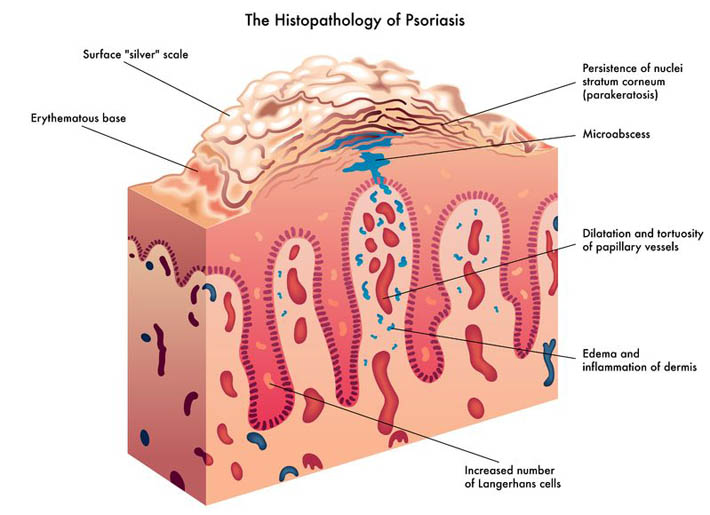
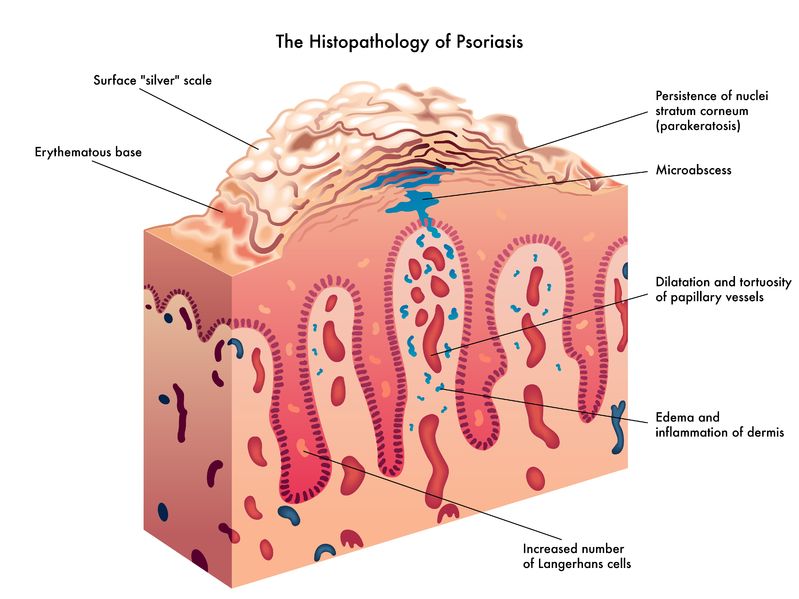
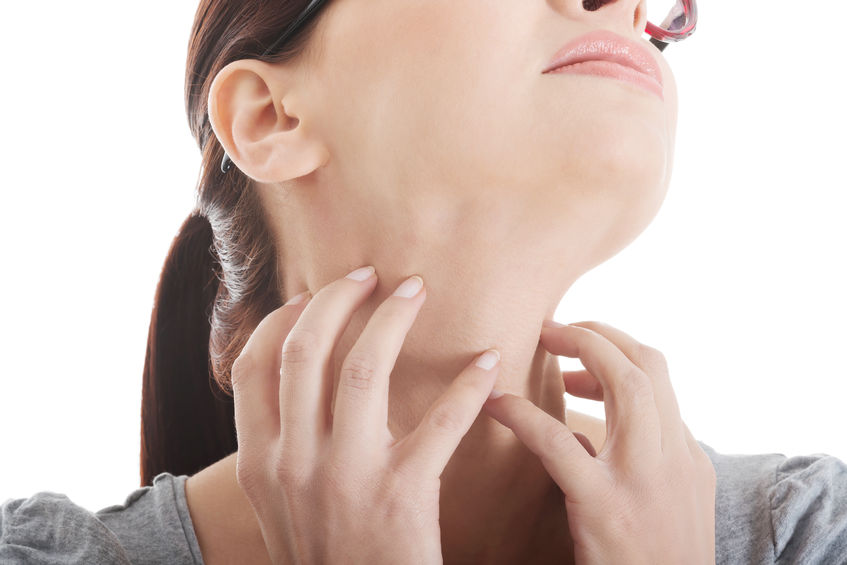 皮膚炎としても知られるアトピー性皮膚炎は慢性で再発性の炎症性皮膚疾患ですが、この疾患はしばしば幼年期に始まり成人期まで続きます[1-3]。世界アレルギー協会によると、“アトピー性”という用語は、アレルギー反応を発症し、(通常はタンパク質の)アレルゲンへの曝露に反応して免疫グロブリンE抗体を生産するような、遺伝性素因を意味します[1-2,4]。皮膚炎は、食物アレルギー、季節性アレルギーや喘息のような数々のアトピー性病態と関連がありますが、これらのアレルギーは共通の病因を持つことが示唆されており、これらの病態の家族歴を持つ人々でより起こりやすいのです[1,3]。しかし、全ての湿疹性皮疹が、ツタの毒による発疹あるいは化学物質・刺激物との接触による発疹(両者とも接触性皮膚炎)のようなアトピー性のものではありません。この記事の主旨として、アトピー性皮膚炎および皮膚炎を置き換え可能なものとして扱います。17 6月 1605 6月 1403 1月 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201401){ ?> download pdf16 5月 1630 4月 17パーキンソン病(PD)は、最も一般的な神経変性疾患の一つで、年齢65歳を超える人々の1-2%が罹患しています。パーキンソン病は、安静時の震え、歩行、椅子に座る・立ち上がるのが困難、振り向きが困難、筋肉の強張り、表情の変化、筆跡の縮小、その他多数の運動症状を呈します。非運動症状も一般的で、それらには、便秘、嗅覚消失、起立性低血圧症、疲労、抑うつ、不安、そして-特に-睡眠異常が含まれます。05 8月 1403 5月 1707 5月 1503 1月 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201401){ ?> download pdf08 6月 1502 9月 1511 9月 1406 10月 1403 7月 1910 4月 16
皮膚炎としても知られるアトピー性皮膚炎は慢性で再発性の炎症性皮膚疾患ですが、この疾患はしばしば幼年期に始まり成人期まで続きます[1-3]。世界アレルギー協会によると、“アトピー性”という用語は、アレルギー反応を発症し、(通常はタンパク質の)アレルゲンへの曝露に反応して免疫グロブリンE抗体を生産するような、遺伝性素因を意味します[1-2,4]。皮膚炎は、食物アレルギー、季節性アレルギーや喘息のような数々のアトピー性病態と関連がありますが、これらのアレルギーは共通の病因を持つことが示唆されており、これらの病態の家族歴を持つ人々でより起こりやすいのです[1,3]。しかし、全ての湿疹性皮疹が、ツタの毒による発疹あるいは化学物質・刺激物との接触による発疹(両者とも接触性皮膚炎)のようなアトピー性のものではありません。この記事の主旨として、アトピー性皮膚炎および皮膚炎を置き換え可能なものとして扱います。17 6月 1605 6月 1403 1月 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201401){ ?> download pdf16 5月 1630 4月 17パーキンソン病(PD)は、最も一般的な神経変性疾患の一つで、年齢65歳を超える人々の1-2%が罹患しています。パーキンソン病は、安静時の震え、歩行、椅子に座る・立ち上がるのが困難、振り向きが困難、筋肉の強張り、表情の変化、筆跡の縮小、その他多数の運動症状を呈します。非運動症状も一般的で、それらには、便秘、嗅覚消失、起立性低血圧症、疲労、抑うつ、不安、そして-特に-睡眠異常が含まれます。05 8月 1403 5月 1707 5月 1503 1月 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201401){ ?> download pdf08 6月 1502 9月 1511 9月 1406 10月 1403 7月 1910 4月 16
月刊ニュースレター
サブスクリプションを保存できませんでした。もう一度やり直してください。
サブスクリプションは成功しました。