Related Articles
- 17 Janv 19Les maladies cardiaques, ou maladies cardiovasculaires (MCV) constituent la première cause de mortalité dans les sociétés occidentales, étant responsables d’environ 1 décès sur 4 aux États-Unis. L’Organisation mondiale de la santé classe également les maladies cardiaques au premier rang des causes de décès dans le monde, 85 % des décès par MCV étant provoqués par une crise cardiaque ou un accident vasculaire cérébral (AVC).
- 16 Mars 19Alors que l’hiver 2019 bat son plein, la grippe et sa cohorte de symptômes sont au rendez-vous. Le froid nous contraint à rester à l’intérieur, nous exposant à échanger nos bactéries, nos virus et autres agents pathogènes mutuels. Vous rappelez-vous cet inconnu que vous avez croisé dans le métro ? Oui, celui avec une toux sèche, le nez qui coule, les yeux rouges et larmoyants, de la fièvre, des frissons, des courbatures, et autres manifestations déplaisantes...
- 23 Août 15Les infections des voies urinaires inférieures que nous appellerons IU dans cet article sont responsables de milliers de rendez-vous médicaux annuellement, car les voies urinaires se situent au deuxième rang en termes de fréquence d’infection. Le terme infection urinaire fait allusion à la présence du nombre de bactéries dans l’urine, soit en général plus de 100 000/ml.
- 06 Déc 18À une époque où les injonctions concernant l’alimentation et la forme physique submergent en permanence le grand public, je crois qu’il est temps de faire une distinction entre un trouble de l’alimentation réel, clinique, et une consommation normale qui suit les représentations sociales alimentaires et corporelles – ce sont deux choses bien différentes.
- 06 Déc 18Vous sentez-vous parfois ballonné ou constipé ? Peut-être éprouvez-vous des maux de tête, ou des réactions cutanées, sans raison apparente ? Êtes-vous en permanence fatigué, incapable de vous concentrer ? L’origine de ces réactions pourrait bien vous surprendre, et est peut-être à chercher dans votre assiette.
- 08 Nov 17
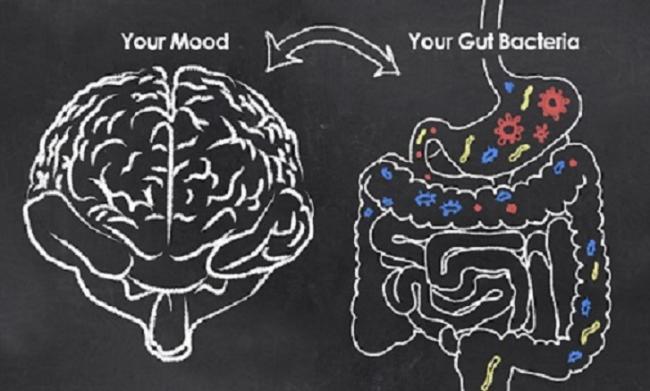
 Pour beaucoup de gens, les maladies mentales suscitent bon nombre d’interrogations sans réponse. Dans mon cas, la question « Pourquoi moi ? » est l’une de celles que je me suis posées très souvent. Elle est même devenue la question centrale de mon engagement de médecin naturopathe spécialisée en santé mentale, me demandant d’où viennent les maladies mentales.
Pour beaucoup de gens, les maladies mentales suscitent bon nombre d’interrogations sans réponse. Dans mon cas, la question « Pourquoi moi ? » est l’une de celles que je me suis posées très souvent. Elle est même devenue la question centrale de mon engagement de médecin naturopathe spécialisée en santé mentale, me demandant d’où viennent les maladies mentales. - 07 Nov 17
- 08 Nov 17
- 24 Sept 18Le battage médiatique de ces dernières années au sujet des « superaliments » a conduit beaucoup d’entre nous à ajouter, un peu au hasard, des fruits secs et autres ingrédients à notre alimentation quotidienne, sans bien comprendre le pourquoi ni le comment. Divers aliments deviennent « tendance » puis passent de mode, et nous nous nous sentons coupables de ne pas les ajouter aussitôt à notre liste de courses. Mais plutôt que de parler de « superaliments », peut-être devrions-nous nous intéresser à ce que sont les « antioxydants », ainsi qu’à leur utilité.
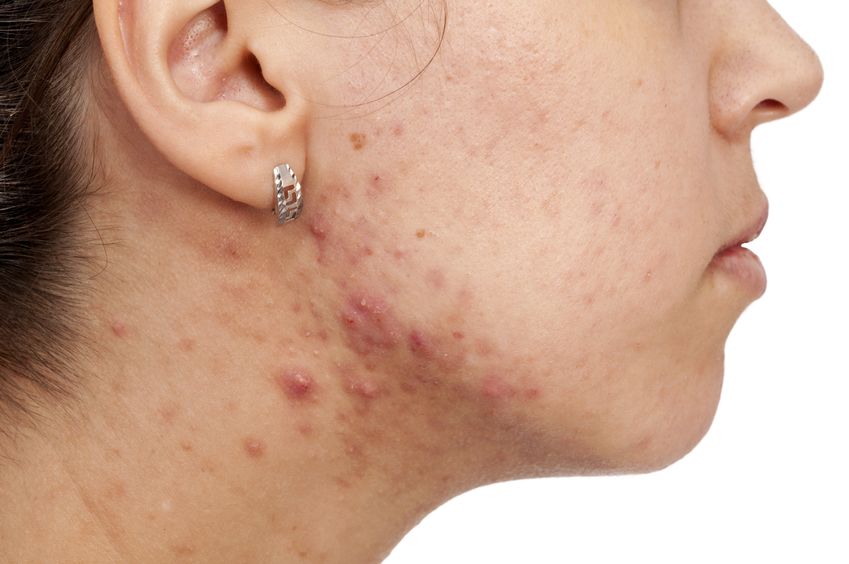
- 09 Mai 19L’acné est l’une des maladies cutanées chroniques les plus répandues : 80 à 90% de la population est touchée, un jour ou l’autre, par l’acné [1]. Il s’agit d’une affection relativement bénigne, qui peut pourtant avoir des effets très lourds sur la santé psychique. On observe, indépendamment de sa gravité, un taux plus élevé d’anxiété et de dépression chez les personnes qui en sont atteintes [2]. Alors même que les lésions acnéiques ont disparu, les cicatrices et traces pigmentaires qui peuvent subsister ont parfois un impact durable sur l’estime de soi et le bien-être psychologique. Ces seules raisons justifient que l’on recherche des solutions efficaces pour lutter contre l’acné.
- 17 Janv 19Nous avons tous entendu dire que la peau est l’organe le plus étendu de notre corps. Elle joue un rôle crucial pour nous protéger des agents pathogènes, pour nous aider à éliminer nos déchets organiques, réguler notre température corporelle, et communiquer des informations grâce au sens du toucher. Il s’agit d’un organe complexe, affecté par notre environnement interne et externe, et dont on ne peut parler sans parler aussi d’autres systèmes organiques.
- 16 Mars 19Plus de 50% des femmes souffriront au cours de leur vie d’une infection urinaire (IU). Entre un tiers et la moitié de ces femmes auront une IU récurrente d’ici un an. Une IU est dite récurrente lorsqu’elle survient au moins trois fois sur une période de 12 mois [1]. Les antibiotiques constituent le traitement le plus couramment utilisé contre ces affections, mais leur usage répétitif entraine une résistance aux antibiotiques qui suscite une prise de conscience et une inquiétude grandissantes. Cette préoccupation explique l’intérêt pour les traitements alternatifs contre les IU. Nous allons parler de ces affections, de leurs causes, et des moyens alternatifs pour les prévenir et les soigner.
- 30 Oct 18Vos règles sont en retard, vraiment en retard. Vous n’êtes pourtant pas enceinte, ni en phase de ménopause. Vous avez peut-être manqué un cycle, ou plusieurs. Naturellement, c’est inquiétant : la plupart des femmes dont les règles ne se décident pas à apparaitre font des tests de grossesse répétés, pour se rassurer. Mais les raisons qui peuvent expliquer l’absence des règles vont bien au-delà d’une éventuelle grossesse.
- 16 Mars 19Le déséquilibre hormonal est un problème de santé auquel beaucoup de femmes sont confrontées. Celles-ci sont amenées à prendre de plus en plus de responsabilités – elles prodiguent des soins, s’occupent des enfants, en plus de travailler pour joindre les deux bouts. Elles sont en conséquence exposées à un stress de plus en plus important, une des principales raisons de l’augmentation des déséquilibres hormonaux. L’exposition aux xéno-œstrogènes dans les produits ménagers (les emballages en plastique), dans les produits de soins, voire dans l’eau du robinet, peut contribuer aux déséquilibres hormonaux, de même que de mauvais choix alimentaires. Ces déséquilibres proviennent de changements dans les taux relatifs d’œstrogènes, de progestérone et/ou de testostérone : les œstrogènes peuvent être trop élevés par rapport à la progestérone, ou la progestérone être trop faible, faisant paraitre élevé le taux d’œstrogènes. Notre article se concentrera sur ces déséquilibres entre progestérone et œstrogènes.
- 23 juil 18Beaucoup de patients viennent me consulter pour des maladies qui affectent leur qualité de vie mais pour lesquelles il n’existe que peu ou pas de solution « standard ». Des symptômes tels qu’une fatigue qui s’aggrave progressivement, une prise de poids, des éruptions cutanées, des maux de tête et des douleurs articulaires sont fréquents. Ces symptômes restent souvent inexpliqués par la médecine conventionnelle pour ce qui est de leur origine, et ne sont pas pris en charge, ou ne le sont que de façon insuffisante, par les traitements pharmaceutiques. Bien que ces traitements soient essentiels dans de nombreuses circonstances, ils ne sont trop souvent, pour ces symptômes chroniques, pas la meilleure solution.
- 30 Nov 18L’inflammation est devenue un sujet d’actualité pour le monde médical, faisant l’objet de recherches croissantes. On pensait naguère que l’arthrite et l’inflammation articulaire commençaient et finissaient dans les articulations, sans autres influences ni connexions. Nous savons aujourd’hui qu’une inflammation intestinale peut avoir des effets sur l’inflammation articulaire, augmenter le risque de diabète, provoquer des poussées d’eczéma, et même déclencher anxiété et dépression dans le cerveau [1]. Les choses sont donc un peu plus complexes qu’on ne le supposait, et prennent nettement plus de temps à corriger, mais le savoir c’est le pouvoir, et la prise de conscience est la première étape vers le progrès.
- 16 Févr 19Les toxines nous entourent. Que ce soit les gaz de votre voiture, votre diner surgelé ou les pensées négatives au travail, les toxines sont partout.
- 16 Janv 19Une bonne partie des personnes qui consultent un médecin naturopathe le font principalement pour des problèmes digestifs. Après des mois d’examens et d’analyses, leur médecin conventionnel les a laissées sans réponse claire, et elles sont à la recherche d’un nouveau point de vue. D’autres fois, leurs examens d’imagerie révèlent quelque chose d’important, mais le système médical est malgré tout à court d’options thérapeutiques.
- 30 Oct 18La polyarthrite rhumatoïde (PR) est une affection chronique relativement répandue. Il s’agit d’une forme d’inflammation articulaire chronique qui peut avoir un impact important sur la qualité de vie. On ne sait pas précisément ce qui provoque la polyarthrite rhumatoïde, mais l’affection présente une composante auto-immune significative. Elle diffère en cela nettement de l’arthrose, bien plus fréquente, qui est plutôt une arthrite d’usure provoquée par l’utilisation mécanique des articulations au cours d’une vie longue et active. La polyarthrite rhumatoïde n’affecte pas seulement les articulations, mais s’accompagne de symptômes inflammatoires systémiques.
- 24 Sept 18Parlons un peu des thérapies nutritionnelles par injection intraveineuse, une option généralement sous-estimée pour traiter de nombreuses affections chroniques. Bien menée, une thérapie nutritionnelle par injection est sans risque, économique, et peut se révéler étonnamment efficace dans certains cas des plus tenaces.
Actualités
Votre abonnement n'a pas pu être enregistré. Veuillez réessayer.
Vous vous êtes abonné avec succès à l’infolettre de Naturopathic Currents.
Les plus populaires
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13
- 16 juin 13
- 17 juin 13
- 17 juin 13
- 17 juin 13
- 01 juil 13