Related Articles
- 10 Mar 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201403){ ?> download pdf
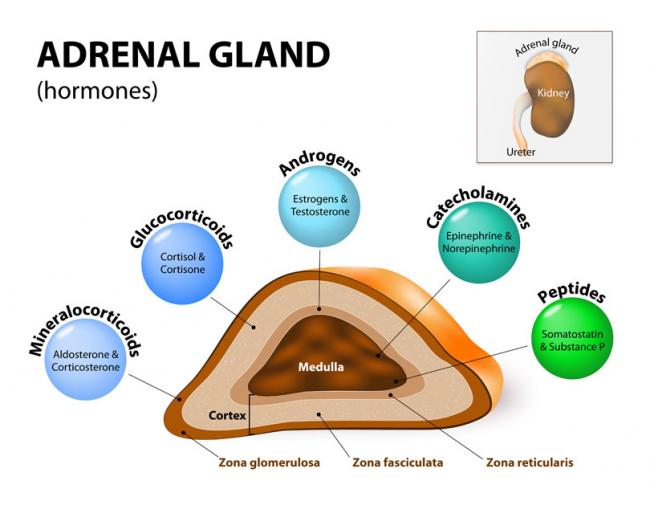
 El síndrome de ovario poliquístico (SOP) es una enfermedad que consiste en la disfunción ovulatoria e hiperandrogenismo, que se define como el exceso de actividad de la testosterona y hormonas andrógenas relacionadas. El SOP afecta aproximadamente al 10% de las mujeres en edad reproductiva, y es una causa común de infertilidad. Sin embargo, las mujeres con SOP a menudo sufren de trastornos más sutiles en otras hormonas eje, así, como la tiroides y las suprarrenales. Este artículo explorará el papel de estos sistemas hormonales en la infertilidad asociada con el síndrome de ovario poliquístico. Comenzamos con una descripción de los problemas del síndrome de ovario poliquístico, así como las terapias basadas en cambios del estilo de vida, que debería ser el tratamiento de primera línea para todas las mujeres con SOP.31 Mayo 16¿Estresada? En el mundo de hoy, a menudo escuchamos que nuestras glándulas suprarrenales están agotadas y no tienen un rendimiento óptimo. Por lo general, atribuimos esto a factores estresantes externos tales como la sobrecarga de trabajo, las responsabilidades emocionales, las responsabilidades de las relaciones personales o las tensiones financieras.30 Jun 18La disponibilidad de los métodos anticonceptivos ha sido un apoyo increíble a la autonomía de las mujeres sobre su salud reproductiva. Como mujeres, hemos gozado de esta maravillosa oportunidad de tener el control de nuestros cuerpos; ya sea para prevenir un embarazo accidental, o para obtener alivio de la disfunción hormonal.14 Mar 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201403){ ?> download pdf
El síndrome de ovario poliquístico (SOP) es una enfermedad que consiste en la disfunción ovulatoria e hiperandrogenismo, que se define como el exceso de actividad de la testosterona y hormonas andrógenas relacionadas. El SOP afecta aproximadamente al 10% de las mujeres en edad reproductiva, y es una causa común de infertilidad. Sin embargo, las mujeres con SOP a menudo sufren de trastornos más sutiles en otras hormonas eje, así, como la tiroides y las suprarrenales. Este artículo explorará el papel de estos sistemas hormonales en la infertilidad asociada con el síndrome de ovario poliquístico. Comenzamos con una descripción de los problemas del síndrome de ovario poliquístico, así como las terapias basadas en cambios del estilo de vida, que debería ser el tratamiento de primera línea para todas las mujeres con SOP.31 Mayo 16¿Estresada? En el mundo de hoy, a menudo escuchamos que nuestras glándulas suprarrenales están agotadas y no tienen un rendimiento óptimo. Por lo general, atribuimos esto a factores estresantes externos tales como la sobrecarga de trabajo, las responsabilidades emocionales, las responsabilidades de las relaciones personales o las tensiones financieras.30 Jun 18La disponibilidad de los métodos anticonceptivos ha sido un apoyo increíble a la autonomía de las mujeres sobre su salud reproductiva. Como mujeres, hemos gozado de esta maravillosa oportunidad de tener el control de nuestros cuerpos; ya sea para prevenir un embarazo accidental, o para obtener alivio de la disfunción hormonal.14 Mar 14'; $link = url($path, array('absolute' => TRUE)); $nid = arg(1); if ($nid == 201403){ ?> download pdf El número de parejas que sufren de infertilidad y / o recurren a técnicas de reproducción asistida (TRA) está en aumento (1). En un estudio publicado en 2012 se encontró que entre parejas canadienses (mujeres de entre 18-4 años), la prevalencia de infertilidad osciló entre 11-15%, y esto representó un aumento en comparación con las estadísticas anteriores (2). Comparando los datos obtenidos, en 1984 la prevalencia de la infertilidad entonces era sólo del 5% (2). Hay muchos factores que son responsables de este aumento, incluyendo el retraso en la maternidad y el aumento de la edad promedio en que las mujeres que intentan concebir; en comparación con 1984, cuando sólo el 3% de los niños primogénitos fueron de madres de 35 y más años de edad, en 2008 el 11% de los primogénitos fueron de madres 35 años o más .
30 Sep 15La menopausia es una transición natural que atraviesan todas las mujeres; significa el comienzo de la etapa de la vida en la que las mujeres ya no tienen su período (1).06 Oct 1431 Ago 15Los fibromas uterinos (también conocidos como leiomiomas) son tumores pélvicos sólidos compuestos de tejido conectivo y músculo (1).31 Dic 16La píldora anticonceptiva oral combinada (PAOC) normalmente es una combinación de estrógeno y progestina que se toma por vía oral para prevenir la fertilidad femenina y el embarazo.31 Oct 16La endometriosis es un trastorno caracterizado por la presencia de tejido endometrial en lugares del cuerpo fuera del útero. Estas lesiones de tejido responden a estímulos hormonales, como los estrógenos, y pueden ser la causa de un dolor pélvico extremo en muchas mujeres.30 Sep 16No hay duda de que su médico de familia cree firmemente en el "cuidado de la salud preconcepcional", que es la atención y asesoramiento que le ayudará tanto a usted como a su pareja a alcanzar un estado de salud óptimo antes de concebir a sus hijos.31 Mayo 17El parto es uno de los procesos más transformadores que una mujer puede experimentar.31 Oct 17La diabetes gestacional (GDM, por sus siglas en inglés) es un diagnóstico que describe la intolerancia a la glucosa con inicio de diabetes durante el embarazo en una mujer que anteriormente no era diabética. [1]31 Ago 18La mayoría de las mujeres pasan toda su vida esperando que termine su ciclo menstrual.31 Mayo 16Ya sea por medios naturales sin mediación, por inducción o por cesárea, el nacimiento de un niño puede ser una experiencia emocionante, aterradora y abrumadora, ¡y todo esto es justo en los primeros momentos de vida!07 Mayo 15
El número de parejas que sufren de infertilidad y / o recurren a técnicas de reproducción asistida (TRA) está en aumento (1). En un estudio publicado en 2012 se encontró que entre parejas canadienses (mujeres de entre 18-4 años), la prevalencia de infertilidad osciló entre 11-15%, y esto representó un aumento en comparación con las estadísticas anteriores (2). Comparando los datos obtenidos, en 1984 la prevalencia de la infertilidad entonces era sólo del 5% (2). Hay muchos factores que son responsables de este aumento, incluyendo el retraso en la maternidad y el aumento de la edad promedio en que las mujeres que intentan concebir; en comparación con 1984, cuando sólo el 3% de los niños primogénitos fueron de madres de 35 y más años de edad, en 2008 el 11% de los primogénitos fueron de madres 35 años o más .
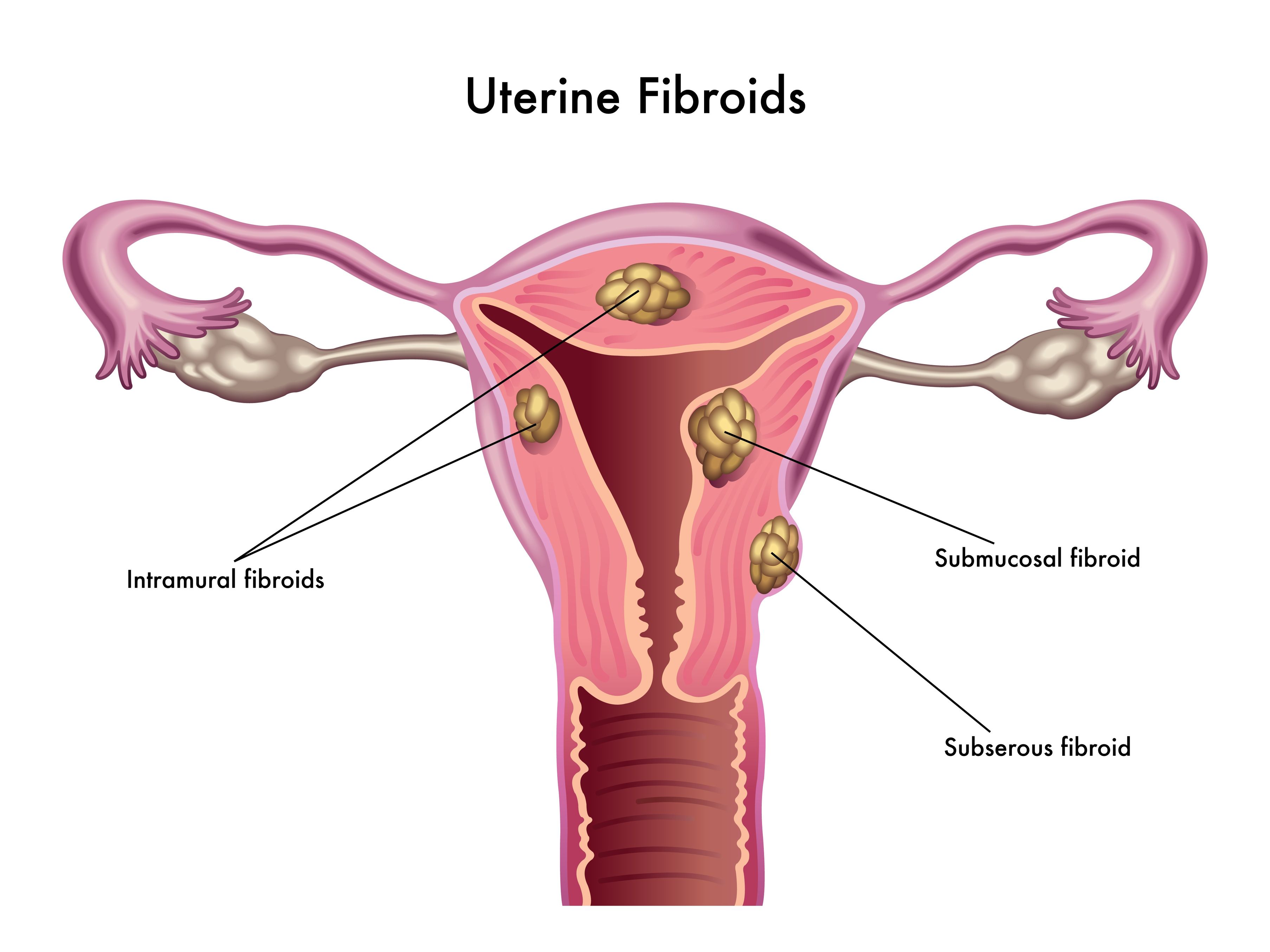
30 Sep 15La menopausia es una transición natural que atraviesan todas las mujeres; significa el comienzo de la etapa de la vida en la que las mujeres ya no tienen su período (1).06 Oct 1431 Ago 15Los fibromas uterinos (también conocidos como leiomiomas) son tumores pélvicos sólidos compuestos de tejido conectivo y músculo (1).31 Dic 16La píldora anticonceptiva oral combinada (PAOC) normalmente es una combinación de estrógeno y progestina que se toma por vía oral para prevenir la fertilidad femenina y el embarazo.31 Oct 16La endometriosis es un trastorno caracterizado por la presencia de tejido endometrial en lugares del cuerpo fuera del útero. Estas lesiones de tejido responden a estímulos hormonales, como los estrógenos, y pueden ser la causa de un dolor pélvico extremo en muchas mujeres.30 Sep 16No hay duda de que su médico de familia cree firmemente en el "cuidado de la salud preconcepcional", que es la atención y asesoramiento que le ayudará tanto a usted como a su pareja a alcanzar un estado de salud óptimo antes de concebir a sus hijos.31 Mayo 17El parto es uno de los procesos más transformadores que una mujer puede experimentar.31 Oct 17La diabetes gestacional (GDM, por sus siglas en inglés) es un diagnóstico que describe la intolerancia a la glucosa con inicio de diabetes durante el embarazo en una mujer que anteriormente no era diabética. [1]31 Ago 18La mayoría de las mujeres pasan toda su vida esperando que termine su ciclo menstrual.31 Mayo 16Ya sea por medios naturales sin mediación, por inducción o por cesárea, el nacimiento de un niño puede ser una experiencia emocionante, aterradora y abrumadora, ¡y todo esto es justo en los primeros momentos de vida!07 Mayo 15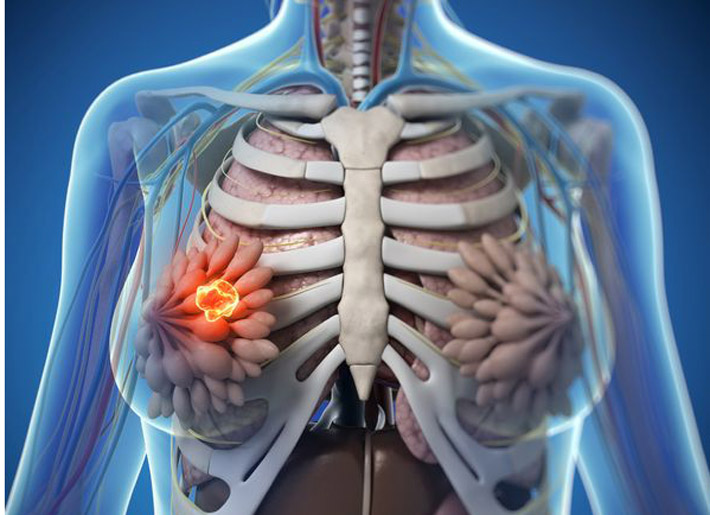 Los senos fibroquísticos se caracterizan como 'bultos' o 'quistes' que se encuentran dentro de la mama. Los senos fibroquísticos surgen del predominio de estrógenos y la deficiencia de progesterona que resulta en una hiper-proliferación de tejido conectivo. Esta condición puede ser asintomática o puede presentar con una nodularidad de la mama, hinchazón y dolor. .30 Nov 15A menudo expresamos quiénes somos y cómo nos sentimos a través de nuestro cabello.30 Abr 17Los problemas de fertilidad asociados con el envejecimiento de la madre son una preocupación cada vez mayor para aquellas que desean concebir.30 Abr 16Toda mujer, si vive lo suficiente, tendrá la menopausia. Para algunas, la transición es fácil e incluso puede ser un alivio de los problemas de un ciclo menstrual regular. Para otras, el cambio es extremadamente difícil ya que luchan por controlar los frecuentes "bochornos", el aumento de peso y la depresión severa.30 Sep 16Puede que haya observado alguna vez, en la televisión o en la realidad, a una mujer con constantes cambios de humor desesperada por helado o chocolate y contestando de mala manera a cualquier comentario provocador con respecto a su comportamiento en "esos días del mes", o tal vez haya sido testigo de alguna otra situación parecida.31 Ene 16El síndrome de ovario poliquístico (SOP) es la causa más frecuente de infertilidad anovulatoria en el 5-10% de las mujeres en edad reproductiva.
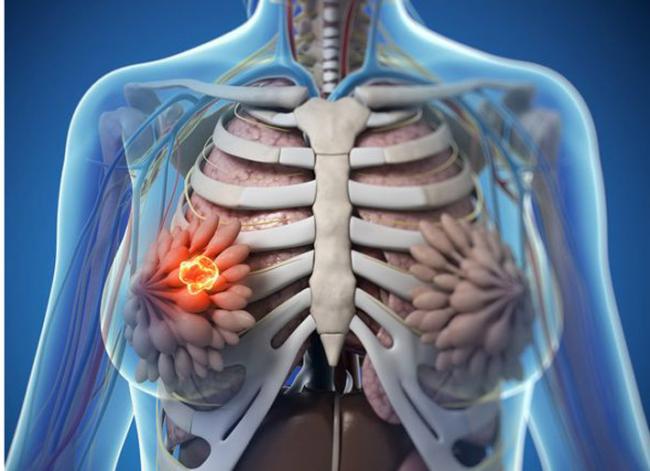
Los senos fibroquísticos se caracterizan como 'bultos' o 'quistes' que se encuentran dentro de la mama. Los senos fibroquísticos surgen del predominio de estrógenos y la deficiencia de progesterona que resulta en una hiper-proliferación de tejido conectivo. Esta condición puede ser asintomática o puede presentar con una nodularidad de la mama, hinchazón y dolor. .30 Nov 15A menudo expresamos quiénes somos y cómo nos sentimos a través de nuestro cabello.30 Abr 17Los problemas de fertilidad asociados con el envejecimiento de la madre son una preocupación cada vez mayor para aquellas que desean concebir.30 Abr 16Toda mujer, si vive lo suficiente, tendrá la menopausia. Para algunas, la transición es fácil e incluso puede ser un alivio de los problemas de un ciclo menstrual regular. Para otras, el cambio es extremadamente difícil ya que luchan por controlar los frecuentes "bochornos", el aumento de peso y la depresión severa.30 Sep 16Puede que haya observado alguna vez, en la televisión o en la realidad, a una mujer con constantes cambios de humor desesperada por helado o chocolate y contestando de mala manera a cualquier comentario provocador con respecto a su comportamiento en "esos días del mes", o tal vez haya sido testigo de alguna otra situación parecida.31 Ene 16El síndrome de ovario poliquístico (SOP) es la causa más frecuente de infertilidad anovulatoria en el 5-10% de las mujeres en edad reproductiva.
Boletín
No se pudo guardar su suscripción. Inténtalo de nuevo.
Su suscripción ha sido exitosa.
Más popular
- 16 Jun 13
- 17 Jun 13
- 17 Jun 13
- 16 Jun 13
- 01 Jul 13
- 16 Jun 13
- 17 Jun 13
- 17 Jun 13
- 16 Jun 13
- 01 Jul 13
- 16 Jun 13
- 17 Jun 13
- 17 Jun 13
- 16 Jun 13
- 01 Jul 13