Related Articles
- 08 Gen 15
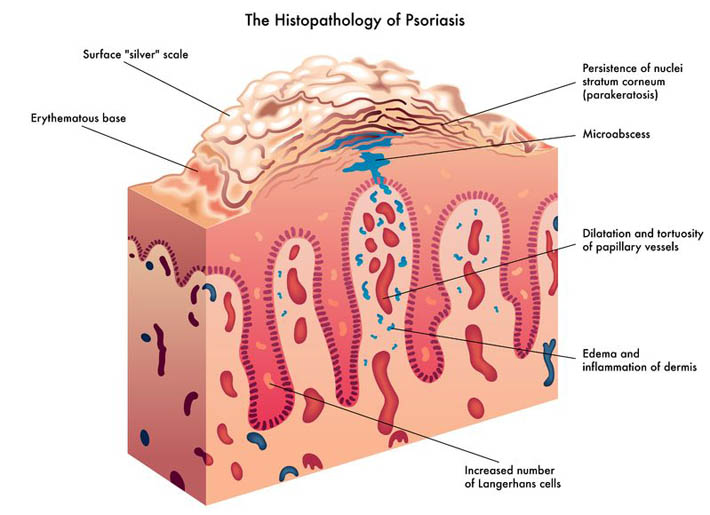
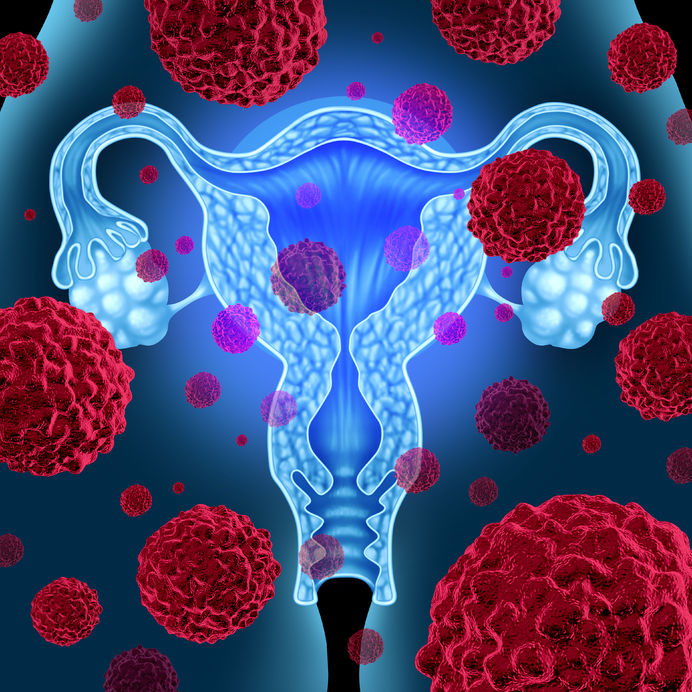 Con il termine displasia cervicale si indica la presenza di cellule anomale considerate premaligne sulla superficie della cervice che possono progredire verso il cancro (1). La displasia cervicale è causata in primo luogo da un'infezione trasmessa sessualmente con diversi ceppi del papilloma virus umano (HPV).
Con il termine displasia cervicale si indica la presenza di cellule anomale considerate premaligne sulla superficie della cervice che possono progredire verso il cancro (1). La displasia cervicale è causata in primo luogo da un'infezione trasmessa sessualmente con diversi ceppi del papilloma virus umano (HPV). - 05 Ott 16
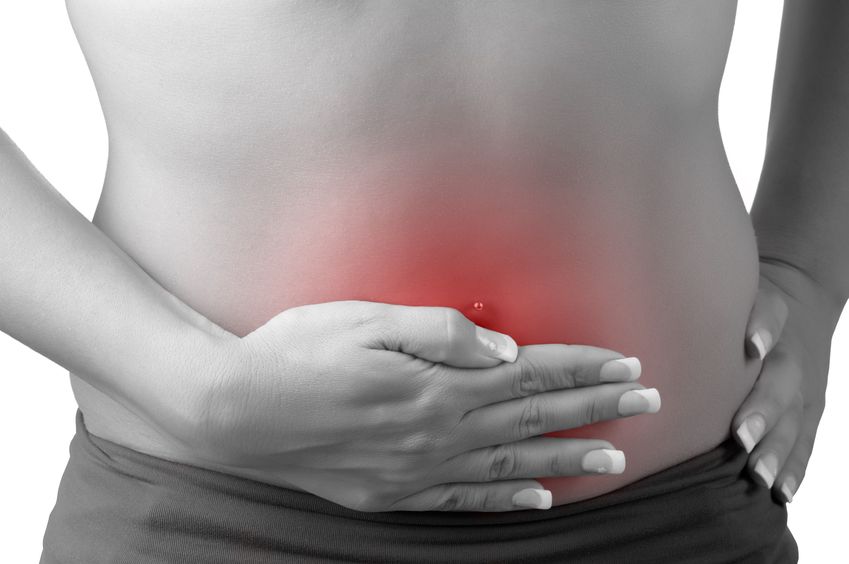
 L’endometriosi è un disturbo caratterizzato dalla presenza di tessuto endometriale in punti del corpo fuori dall’utero. Queste lesioni del tessuto rispondono a stimoli ormonali, come estrogeni, e possono essere la causa di estremo dolore pelvico per molte donne. Ci sono molti diversi stadi e gravità della patologia: più comunemente le donne riscontrano dismenorrea del ciclo (mestruazioni dolorose o crampi mestruali), dispareunia (dolore durante il rapporto), dischezia (defecazione dolorosa), e/o dolore pelvico cronico non collegato al ciclo.
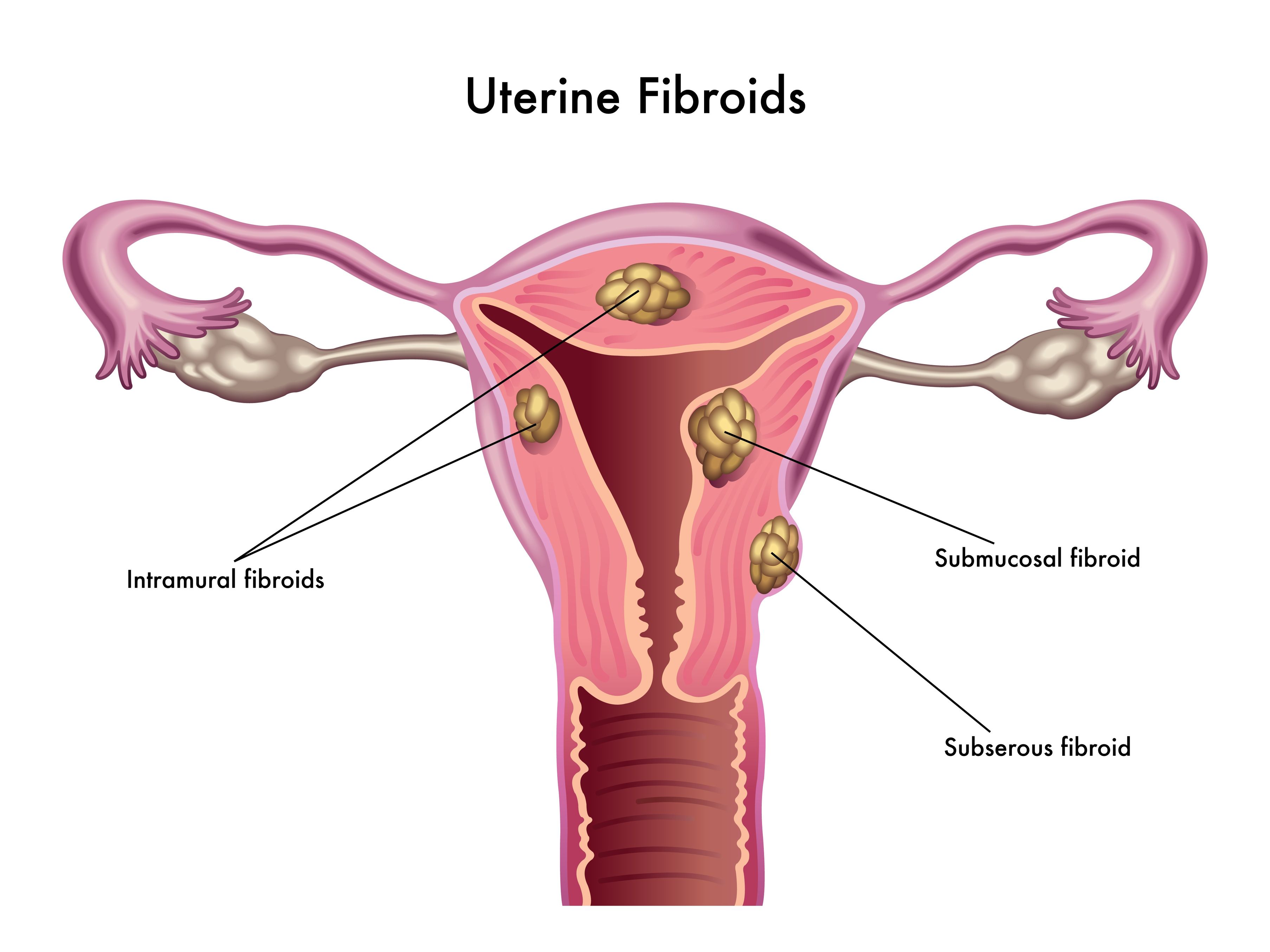
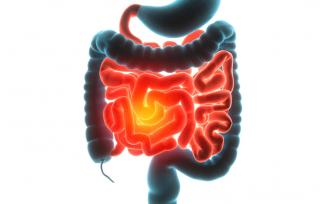
L’endometriosi è un disturbo caratterizzato dalla presenza di tessuto endometriale in punti del corpo fuori dall’utero. Queste lesioni del tessuto rispondono a stimoli ormonali, come estrogeni, e possono essere la causa di estremo dolore pelvico per molte donne. Ci sono molti diversi stadi e gravità della patologia: più comunemente le donne riscontrano dismenorrea del ciclo (mestruazioni dolorose o crampi mestruali), dispareunia (dolore durante il rapporto), dischezia (defecazione dolorosa), e/o dolore pelvico cronico non collegato al ciclo. - 04 Ago 15I fibromi uterini (conosciuti anche come leiomiomi) sono tumori uterini solidi composti da tessuto connettivo e muscolare (1). I leiomiomi variano in termini di dimensioni, forma e posizione; se si accerta la presenza di un leiomioma molto probabilmente ne sono presenti altri. I leiomiomi si distinguono in sottomucosa (sotto l’endometrio), intramurale (nella parete uterina), oppure subserosali (nella parete esterna dell’utero). Possono essere intralegamentosi (nella cervice tra i legamenti della parete stessa), peduncolati e penzolanti da un lembo all’interno della cavità uterina (peduncolati sottomucosi), oppure peduncolati all’esterno della parete uterina (peduncolati). Questi tumori sono di solito i tumori benigni a basso potenziale maligno (2).
- 02 Giu 14
 La gravidanza può essere una delle esperienze più emozionanti della vita di una donna. Tuttavia, essa può anche essere uno dei momenti più stressanti, soprattutto se ci sono complicazioni dovute a questioni di salute. Sono molti gli "effetti collaterali" comuni della gravidanza, come ad esempio nausea, bruciore di stomaco e stanchezza. 30 Set 17Fibromi colpiscono tra il 5% e il 21% della popolazione e possono presentarsi con dolore pelvico non-ciclico, gonfiore addominale, stitichezza, aumento della frequenza urinaria, affaticamento e dispareunia, dolore durante il coito e menorragia, ovvero un flusso mestruale molto pesante (1).06 Apr 16Ogni donna, vivendo a lungo, sperimenterà la menopausa. Per alcuni la transizione è facile e può anche essere un sollievo dai disturbi di un normale ciclo mestruale. Per altri il cambiamento è estremamente impegnativo per via della difficoltà a gestire frequenti "vampate di calore”, l’aumento di peso e una grave depressione. Molti dei sintomi della menopausa possono essere direttamente correlati alla diminuzione della produzione di ormoni sessuali - in particolare gli estrogeni e il progesterone. Sembra ragionevole che il ritorno di questi ormoni ai livelli di premenopausa dovrebbe, e spesso non lo fa, invertire i sintomi e portare ad un senso di benessere generale.05 Set 15La menopausa è una transizione naturale vissuta da tutte le donne; segna l'inizio di una fase di vita durante la quale una donna perde il ciclo mestruale (1). La menopausa si riferisce all’assenza del ciclo mestruale (2). Viene definita come un periodo di tempo di almeno un anno durante il quale una donna manca di ciclo mestruale (1). Segna l’inizio anche dell’infertilità che impedisce definitivamente alle donne la procreazione. Naturalmente la menopausa si verifica quando le ovaie non rispondono più alla stimolazione da parte dell'ipofisi a secernere gli estrogeni e il progesterone (3). Si verifica solitamente nelle donne di età compresa tra i 45 e 55 (2), con un’età media di inizio menopausa di 51 anni. In questo periodo il corpo subisce cambiamenti ormonali che influiscono su ogni donna in modo diverso. Le donne intorno ai quarant’anni soffrono di una riduzione dell’ormone femminile chiamato estrogeno. Di conseguenza, le donne iniziano ad avere cicli mestruali irregolari che a volte si interrompono completamente (1).02 Set 16
La gravidanza può essere una delle esperienze più emozionanti della vita di una donna. Tuttavia, essa può anche essere uno dei momenti più stressanti, soprattutto se ci sono complicazioni dovute a questioni di salute. Sono molti gli "effetti collaterali" comuni della gravidanza, come ad esempio nausea, bruciore di stomaco e stanchezza. 30 Set 17Fibromi colpiscono tra il 5% e il 21% della popolazione e possono presentarsi con dolore pelvico non-ciclico, gonfiore addominale, stitichezza, aumento della frequenza urinaria, affaticamento e dispareunia, dolore durante il coito e menorragia, ovvero un flusso mestruale molto pesante (1).06 Apr 16Ogni donna, vivendo a lungo, sperimenterà la menopausa. Per alcuni la transizione è facile e può anche essere un sollievo dai disturbi di un normale ciclo mestruale. Per altri il cambiamento è estremamente impegnativo per via della difficoltà a gestire frequenti "vampate di calore”, l’aumento di peso e una grave depressione. Molti dei sintomi della menopausa possono essere direttamente correlati alla diminuzione della produzione di ormoni sessuali - in particolare gli estrogeni e il progesterone. Sembra ragionevole che il ritorno di questi ormoni ai livelli di premenopausa dovrebbe, e spesso non lo fa, invertire i sintomi e portare ad un senso di benessere generale.05 Set 15La menopausa è una transizione naturale vissuta da tutte le donne; segna l'inizio di una fase di vita durante la quale una donna perde il ciclo mestruale (1). La menopausa si riferisce all’assenza del ciclo mestruale (2). Viene definita come un periodo di tempo di almeno un anno durante il quale una donna manca di ciclo mestruale (1). Segna l’inizio anche dell’infertilità che impedisce definitivamente alle donne la procreazione. Naturalmente la menopausa si verifica quando le ovaie non rispondono più alla stimolazione da parte dell'ipofisi a secernere gli estrogeni e il progesterone (3). Si verifica solitamente nelle donne di età compresa tra i 45 e 55 (2), con un’età media di inizio menopausa di 51 anni. In questo periodo il corpo subisce cambiamenti ormonali che influiscono su ogni donna in modo diverso. Le donne intorno ai quarant’anni soffrono di una riduzione dell’ormone femminile chiamato estrogeno. Di conseguenza, le donne iniziano ad avere cicli mestruali irregolari che a volte si interrompono completamente (1).02 Set 16 Ci sono pochi dubbi che il vostro medico di famiglia creda fermamente nell’ “assistenza sanitaria al pre-concepimento”, vale a dire la cura e il counseling designati per aiutare voi e il vostro partner ad essere più in salute possibile prima di concepire vostro figlio. In effetti l’assistenza al pre-concepimento è considerata dai medici e dalle autorità in materia di salute generale come molto importante per la fertilità, per i risultati della gravidanza e potenzialmente per la salute futura di vostro figlio quando sarà adulto. 05 Mar 16La candidosi può essere un’infezione estremamente sgradevole e con un impatto significativo sulla qualità della vita di una donna. Il 75% delle donne soffre di candidosi almeno una volta nella vita, il 45% soffre di due o più episodi, e il 5-8% soffre frequentemente di queste infezioni durante la propria vita (5). La candidosi non è classificata come una infezione trasmessa sessualmente (STI), ma può essere trasmessa tra partner durante il rapporto sessuale e ai neonati attraverso il canale uterino durante il parto (1). Anche se non rappresenta un pericolo per la vita, l’improvvisa insorgenza e uno sviluppo rapido della candidosi porta le donne ad affrontare disturbi che riguardano prurito, bruciore, condizione dolorosa, senza sapere come curarla. Inoltre, le ricorrenti candidosi possono influenzare negativamente l’autostima e la fiducia in sé di una donna e di contribuire ad una diminuzione della libido. (9).30 Giu 17Capire il ciclo mestruale comporta più di una semplice stima sul tuo prossimo ciclo. Conoscere il proprio corpo e monitorare i propri cicli mestruali può fornire la comprensione della tua salute ormonale e riproduttiva. Potresti avvertire dei sintomi che noi di solito etichettiamo come "normali", quando dovremmo invece chiamarli "comuni". Questi sintomi potrebbero essere segni di: uno squilibrio ormonale, una carenza di nutrienti, troppo bassa o troppo alta percentuale di grasso corporeo (1), o il risultato dello stress.06 Ott 1406 Mag 16Che sia indotta naturalmente, o con cesareo, la nascita di un bambino può essere un’esperienza eccitante, scioccante e travolgente, e tutto questo accade nei primi momenti di vita! Mentre alcuni parti vanno scrupolosamente pianificati e programmati, altri non sono consueti, e fortunatamente procedure come il parto cesareo (PC) sono a disposizione di coloro che altrimenti potrebbero subire conseguenze negative legate al parto (25). Mentre i parti cesarei vengono solitamente eseguiti quando un parto naturale potenzialmente mette a rischio la vita della madre e del neonato, questi parti sono diventati sempre più diffusi anche nei casi in cui il parto naturale è possibile (25).31 Mag 17Il parto è uno dei processi più trasformativi che una donna possa sperimentare.03 Ago 16
Ci sono pochi dubbi che il vostro medico di famiglia creda fermamente nell’ “assistenza sanitaria al pre-concepimento”, vale a dire la cura e il counseling designati per aiutare voi e il vostro partner ad essere più in salute possibile prima di concepire vostro figlio. In effetti l’assistenza al pre-concepimento è considerata dai medici e dalle autorità in materia di salute generale come molto importante per la fertilità, per i risultati della gravidanza e potenzialmente per la salute futura di vostro figlio quando sarà adulto. 05 Mar 16La candidosi può essere un’infezione estremamente sgradevole e con un impatto significativo sulla qualità della vita di una donna. Il 75% delle donne soffre di candidosi almeno una volta nella vita, il 45% soffre di due o più episodi, e il 5-8% soffre frequentemente di queste infezioni durante la propria vita (5). La candidosi non è classificata come una infezione trasmessa sessualmente (STI), ma può essere trasmessa tra partner durante il rapporto sessuale e ai neonati attraverso il canale uterino durante il parto (1). Anche se non rappresenta un pericolo per la vita, l’improvvisa insorgenza e uno sviluppo rapido della candidosi porta le donne ad affrontare disturbi che riguardano prurito, bruciore, condizione dolorosa, senza sapere come curarla. Inoltre, le ricorrenti candidosi possono influenzare negativamente l’autostima e la fiducia in sé di una donna e di contribuire ad una diminuzione della libido. (9).30 Giu 17Capire il ciclo mestruale comporta più di una semplice stima sul tuo prossimo ciclo. Conoscere il proprio corpo e monitorare i propri cicli mestruali può fornire la comprensione della tua salute ormonale e riproduttiva. Potresti avvertire dei sintomi che noi di solito etichettiamo come "normali", quando dovremmo invece chiamarli "comuni". Questi sintomi potrebbero essere segni di: uno squilibrio ormonale, una carenza di nutrienti, troppo bassa o troppo alta percentuale di grasso corporeo (1), o il risultato dello stress.06 Ott 1406 Mag 16Che sia indotta naturalmente, o con cesareo, la nascita di un bambino può essere un’esperienza eccitante, scioccante e travolgente, e tutto questo accade nei primi momenti di vita! Mentre alcuni parti vanno scrupolosamente pianificati e programmati, altri non sono consueti, e fortunatamente procedure come il parto cesareo (PC) sono a disposizione di coloro che altrimenti potrebbero subire conseguenze negative legate al parto (25). Mentre i parti cesarei vengono solitamente eseguiti quando un parto naturale potenzialmente mette a rischio la vita della madre e del neonato, questi parti sono diventati sempre più diffusi anche nei casi in cui il parto naturale è possibile (25).31 Mag 17Il parto è uno dei processi più trasformativi che una donna possa sperimentare.03 Ago 16 In quanto Medici Naturopati, un’area in cui eccelliamo è il bilanciamento degli ormoni dei nostri pazienti (maschi e femmine). Una comune falsa credenza che le donne hanno riguardo al loro ciclo mestruale è che la pillola anticoncezionale sia prescritta per regolare il loro ciclo. Questo non potrebbe essere più lontano dalla verità. È importante che i professionisti nel campo medico inizino a riferirsi alla pillola anticoncezionale per ciò che essa è: una terapia ormonale soppressiva che va oltre la naturale produzione di ormoni. 30 Giu 18La disponibilità dei contraccettivi per il controllo delle nascite è stata incredibilmente favorevole per l'autonomia delle donne, in merito alla salute riproduttiva. Come donne, ci è stata data questa straordinaria opportunità di controllare i nostri corpi, sia per prevenire una gravidanza accidentale, sia per ottenere sollievo dalla disfunzione ormonale.31 Ott 17Il diabete mellito gestazionale (DGM) è una diagnosi che descrive l’intolleranza al glucosio, con l'insorgenza del diabete durante la gravidanza, in una donna precedentemente non-diabetica. [1] Con una prevalenza di 8-18%, nelle gravidanze canadesi,[2] lo screening è consigliato dopo circa 24 settimane di gestazione.[3]07 Mag 15
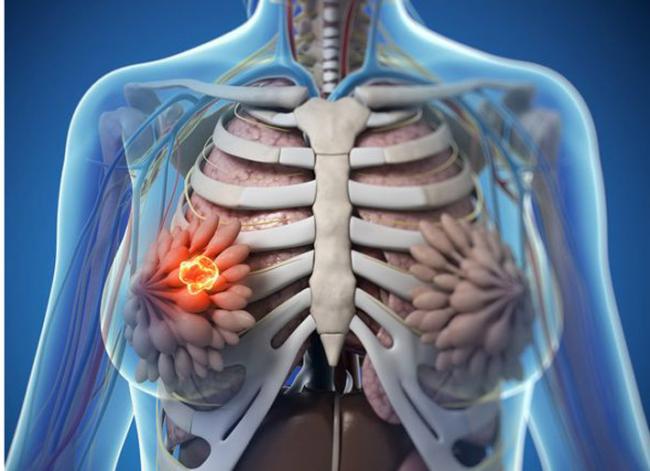
In quanto Medici Naturopati, un’area in cui eccelliamo è il bilanciamento degli ormoni dei nostri pazienti (maschi e femmine). Una comune falsa credenza che le donne hanno riguardo al loro ciclo mestruale è che la pillola anticoncezionale sia prescritta per regolare il loro ciclo. Questo non potrebbe essere più lontano dalla verità. È importante che i professionisti nel campo medico inizino a riferirsi alla pillola anticoncezionale per ciò che essa è: una terapia ormonale soppressiva che va oltre la naturale produzione di ormoni. 30 Giu 18La disponibilità dei contraccettivi per il controllo delle nascite è stata incredibilmente favorevole per l'autonomia delle donne, in merito alla salute riproduttiva. Come donne, ci è stata data questa straordinaria opportunità di controllare i nostri corpi, sia per prevenire una gravidanza accidentale, sia per ottenere sollievo dalla disfunzione ormonale.31 Ott 17Il diabete mellito gestazionale (DGM) è una diagnosi che descrive l’intolleranza al glucosio, con l'insorgenza del diabete durante la gravidanza, in una donna precedentemente non-diabetica. [1] Con una prevalenza di 8-18%, nelle gravidanze canadesi,[2] lo screening è consigliato dopo circa 24 settimane di gestazione.[3]07 Mag 15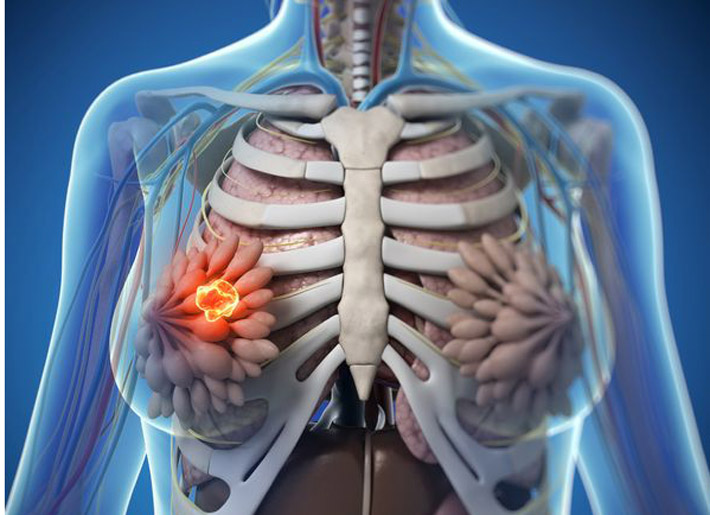 Il seno fibrocistico è caratterizzato dalla presenza di "noduli" o "cisti" nel seno. Il seno fibrocistico ha origine da una predominanza di estrogeni e una carenza di progesterone che comporta un'iper-profilerazione del tessuto connettivo. Questa condizione può essere asintomatica o presentarsi con noduli, gonfiore e dolore al seno .04 Gen 17
Il seno fibrocistico è caratterizzato dalla presenza di "noduli" o "cisti" nel seno. Il seno fibrocistico ha origine da una predominanza di estrogeni e una carenza di progesterone che comporta un'iper-profilerazione del tessuto connettivo. Questa condizione può essere asintomatica o presentarsi con noduli, gonfiore e dolore al seno .04 Gen 17 Le infezioni vaginali portano comunemente le donne a cercare l’aiuto di un medico o ad auto-medicarsi con preparati da banco. È difficile non farsi da sé delle prescrizioni con così tanti trattamenti disponibili per le candidosi. Siamo passati dal trattamento di sette giorni ai tempi di nostra madre o di nostra nonna, alle versioni più semplici e “pulite” del “trattamento da una pastiglia” da assumere sia oralmente che per via vaginale. Pensare di avere una candidosi a causa di un nuovo prurito vaginale, possibile odore e perdite potrebbe essere fuorviante. 06 Set 16
Le infezioni vaginali portano comunemente le donne a cercare l’aiuto di un medico o ad auto-medicarsi con preparati da banco. È difficile non farsi da sé delle prescrizioni con così tanti trattamenti disponibili per le candidosi. Siamo passati dal trattamento di sette giorni ai tempi di nostra madre o di nostra nonna, alle versioni più semplici e “pulite” del “trattamento da una pastiglia” da assumere sia oralmente che per via vaginale. Pensare di avere una candidosi a causa di un nuovo prurito vaginale, possibile odore e perdite potrebbe essere fuorviante. 06 Set 16 Potreste averlo visto tanto in tv quanto nella realtà: una donna particolarmente emotiva che si getta su una vaschetta di gelato o su un pezzo di cioccolata e risponde seccata a ogni provocatorio commento riguardante il suo comportamento in “quei giorni del mese”. La sindrome pre-mestruale, o PMS, è un termine spesso usato umoristicamente per fare riferimento a donne che attraversano quello che può sembrare un esagerato ma naturale sbalzo ormonale prima delle mestruazioni. Al contrario la PMS è effettivamente un disturbo clinico che non tutte le donne provano, ma che colpisce una grossa fetta della popolazione di donne giovani e di mezza età. È caratterizzato da un complesso gioco di sintomi fisici ed emotivi che si verificano durante la fase luteale del ciclo mestruale. 05 Nov 15Lo stato dei nostri capelli è l’espressione di chi siamo e dello stato della nostra salute. Indipendentemente se i capelli sono ricci, lisci, ritorti, intrecciati o raccolti; si tratta di un sinonimo universale di bellezza, sensualità, creatività e avvenenza. Inoltre, riflettono lo stato della nostra salute. Proteggono la testa e la cute, coprendo e al tempo stesso conferendo maggiore personalità. Biochimicamente, riflettono la nostra interiorità e socialmente, ci rendono unici al mondo. Non c’ è da meravigliarsi se l'industria dei capelli complessivamente registri entrate di milioni se non miliardi ogni anno. In tutto il mondo in ogni cultura sono stati eseguiti rituali con i capelli, considerati forse la parte di una persona correlata più di ogni altra alla stima di sé, alla fiducia in sé stessi e alla propria bellezza. Frequentemente utilizziamo frasi legate alla loro influenza esercitata sul nostro umore: "Sto avendo una giornata di brutti capelli!" o "Io amo il modo in cui i miei capelli sembrano”. Pertanto, non è difficile immaginare il perché una persona si preoccupi oppure si angosci quando i capelli iniziano a cadere.
Potreste averlo visto tanto in tv quanto nella realtà: una donna particolarmente emotiva che si getta su una vaschetta di gelato o su un pezzo di cioccolata e risponde seccata a ogni provocatorio commento riguardante il suo comportamento in “quei giorni del mese”. La sindrome pre-mestruale, o PMS, è un termine spesso usato umoristicamente per fare riferimento a donne che attraversano quello che può sembrare un esagerato ma naturale sbalzo ormonale prima delle mestruazioni. Al contrario la PMS è effettivamente un disturbo clinico che non tutte le donne provano, ma che colpisce una grossa fetta della popolazione di donne giovani e di mezza età. È caratterizzato da un complesso gioco di sintomi fisici ed emotivi che si verificano durante la fase luteale del ciclo mestruale. 05 Nov 15Lo stato dei nostri capelli è l’espressione di chi siamo e dello stato della nostra salute. Indipendentemente se i capelli sono ricci, lisci, ritorti, intrecciati o raccolti; si tratta di un sinonimo universale di bellezza, sensualità, creatività e avvenenza. Inoltre, riflettono lo stato della nostra salute. Proteggono la testa e la cute, coprendo e al tempo stesso conferendo maggiore personalità. Biochimicamente, riflettono la nostra interiorità e socialmente, ci rendono unici al mondo. Non c’ è da meravigliarsi se l'industria dei capelli complessivamente registri entrate di milioni se non miliardi ogni anno. In tutto il mondo in ogni cultura sono stati eseguiti rituali con i capelli, considerati forse la parte di una persona correlata più di ogni altra alla stima di sé, alla fiducia in sé stessi e alla propria bellezza. Frequentemente utilizziamo frasi legate alla loro influenza esercitata sul nostro umore: "Sto avendo una giornata di brutti capelli!" o "Io amo il modo in cui i miei capelli sembrano”. Pertanto, non è difficile immaginare il perché una persona si preoccupi oppure si angosci quando i capelli iniziano a cadere.
Newsletter
Le informazioni fornite non sono valide. Controlla il formato del campo e riprova.
La tua iscrizione è andata a buon fine.
Più Popolare
- 17 Giu 13
- 17 Giu 13
- 17 Giu 13
- 01 Lug 13
- 17 Giu 13
- 17 Giu 13
- 17 Giu 13
- 01 Lug 13
- 17 Giu 13
- 17 Giu 13
- 17 Giu 13
- 01 Lug 13