Related Articles
- 06 Dic 18¿Alguna vez te has sentido hinchado o estreñido? ¿Tal vez tienes dolores de cabeza o reacciones en la piel sin causa conocida? ¿Tal vez estás constantemente cansado, no puedes concentrarte o prestar atención? La causa de estas reacciones puede sorprenderte y no tendrás que buscarla más allá de tu cena.
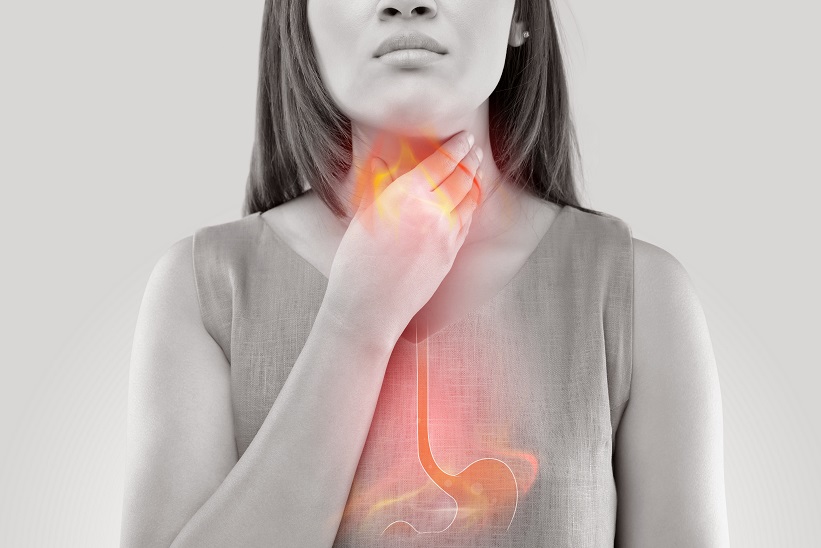
- 06 Dic 18La enfermedad por reflujo gastroesofágico (ERGE) es el flujo en dirección opuesta de los contenidos del estómago hacia el esófago, a menudo llamada también “acidez estomacal” o “reflujo ácido”. La ERGE se produce principalmente debido a un aumento de la presión abdominal o al mal funcionamiento del esfínter esofágico inferior (EEI), que es un conjunto de músculos ubicado en el extremo del esófago donde se encuentra con el estómago.
- 06 Dic 18En esta parte del mundo, se sabe que fumar cigarrillos es perjudicial para la salud y que los efectos del humo que se inhala de modo pasivo son igual de peligrosos para la familia y los amigos. La legislación gubernamental ha obligado a muchas personas a dejar de fumar al hacer que sea más difícil continuar con la adicción, imponiendo un límite de 20 pies (6 m) o 30 pies (9 m) alrededor de la mayoría de los edificios públicos, y prohibiendo fumar dentro de cualquier edificio público. Y aunque las tasas de tabaquismo en los hombres han disminuido del 61% en 1961 al 20% en la actualidad, unos 4,2 millones de canadienses continúan con el hábito y siguen afectando su salud.
- 06 Dic 18En un mundo donde la gente se ve bombardeada constantemente con ideas sobre la alimentación saludable y los cuerpos “en forma”, pareciera importante distinguir entre un trastorno alimenticio verdadero y diagnosticable y un patrón de la sociedad con relación a sus pensamientos sobre la comida y el cuerpo, porque no son lo mismo. ¡Lo que se consideraría “normal” dentro de una cultura que se ha vuelto increíblemente anormal con respecto a la comida / el cuerpo es un tema para otro artículo!
- 14 Ene 21Los productos finales de glicación avanzada (AGEs, por sus siglas en inglés) son compuestos que se generan bajo condiciones de hiperglicemia. Pueden formarse de manera endógena o consumirse a través de la dieta.
- 30 Nov 17Para muchos, la enfermedad mental está plagada de muchas preguntas sin respuesta.
- 30 Nov 17Cuando se trata de niveles de energía, estado de ánimo, memoria y concentración, parece que todos tenemos días buenos y días malos. Pero cuando los días malos parecen superar constantemente los buenos, podría ser una señal de que tu cuerpo está pidiendo ayuda.
- 30 Nov 17Los trastornos alimenticios (incluida la anorexia y la bulimia nerviosa, el trastorno por atracón y el trastorno alimenticio no especificado) siguen siendo increíblemente difíciles de tratar terapéuticamente y continúan siendo muy mal entendidos entre el público en general y la profesión médica.
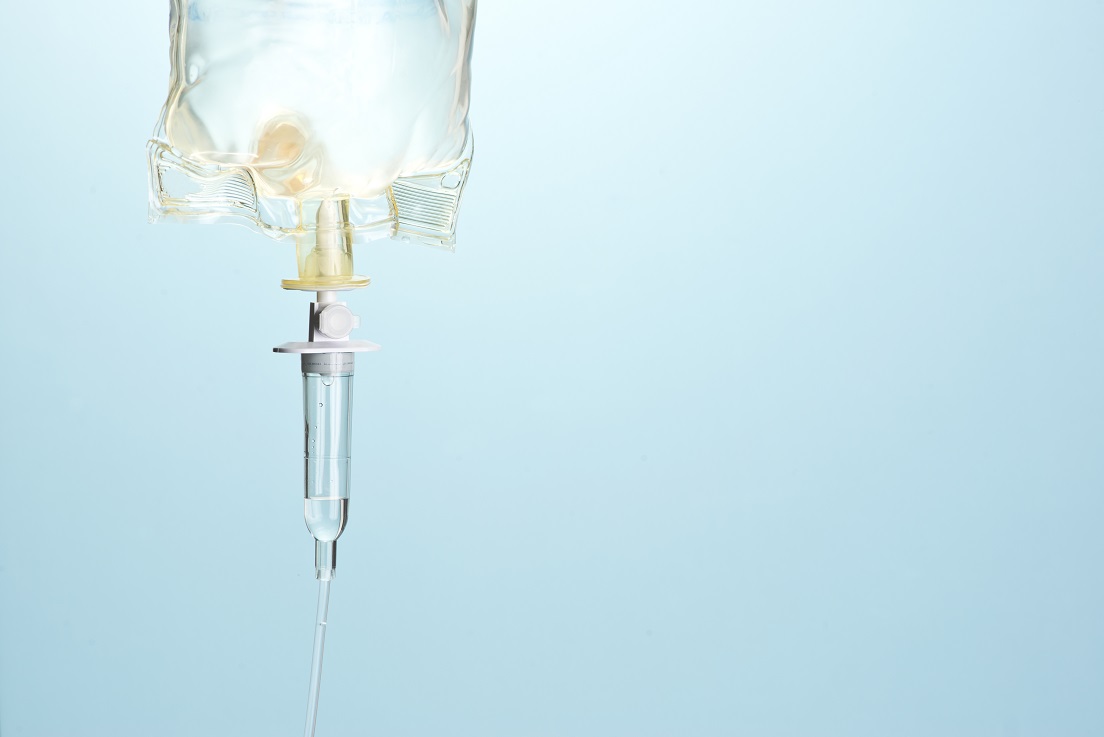
- 30 Sep 18Hablemos de la terapia de nutrientes por vía intravenosa (IV), una opción terapéutica a menudo subvalorada para muchas afecciones crónicas.
- 30 Sep 18El tracto urinario es parte del sistema excretor que elimina los desechos y los metabolitos innecesarios del cuerpo para mantener la homeostasis y el equilibrio bioquímico.
- 30 Abr 19¿Recuerdas la famosa frase: “Una manzana al día mantiene al médico en la lejanía”? Teniendo en cuenta lo altamente nutritivas que son las manzanas, no es una idea descabellada estudiar de qué manera son los alimentos un aliado en la lucha contra las enfermedades crónicas.
- 30 Nov 18La inflamación se ha convertido en un tema candente en el mundo médico, y el conjunto de investigaciones sobre ella sigue creciendo.
- 28 Feb 19Estamos rodeados de toxinas. Las toxinas están en todas partes, en el humo de tu automóvil que inhalas, en la cena congelada que comes o en los pensamientos negativos que tienes en el trabajo.
- 31 Oct 18La fruta es una parte importante de una dieta saludable. Ya sea fresca, congelada, enlatada o seca, el Departamento de Agricultura de los Estados Unidos (USDA, por sus siglas en inglés) recomienda dos porciones de fruta por día,[1] mientras que la Asociación Americana del Corazón (AHA, por sus siglas en inglés) recomienda cuatro porciones por día.[2]
- 09 Mayo 19El acné vulgar es una de las afecciones cutáneas crónicas más comunes. Se estima que del 80 al 90% de la población tendrá algún grado de acné.[1] Aunque es una condición relativamente benigna, puede afectar muy seriamente la salud mental de una persona. Se observan tasas más altas de ansiedad y depresión en las personas con acné, independientemente de la gravedad.[2] Incluso una vez que las lesiones de acné han desaparecido, las cicatrices y los cambios en la pigmentación que posiblemente queden pueden afectar la autoestima y el bienestar psicológico por mucho tiempo. Tan solo por estas razones, encontrar soluciones efectivas para el acné es vital.
- 09 Mayo 19En el embarazo, hay tres trimestres, que abarcan nueve meses. El posparto a veces se conoce como el “cuarto trimestre” y se puede dividir en tres fases distintas.
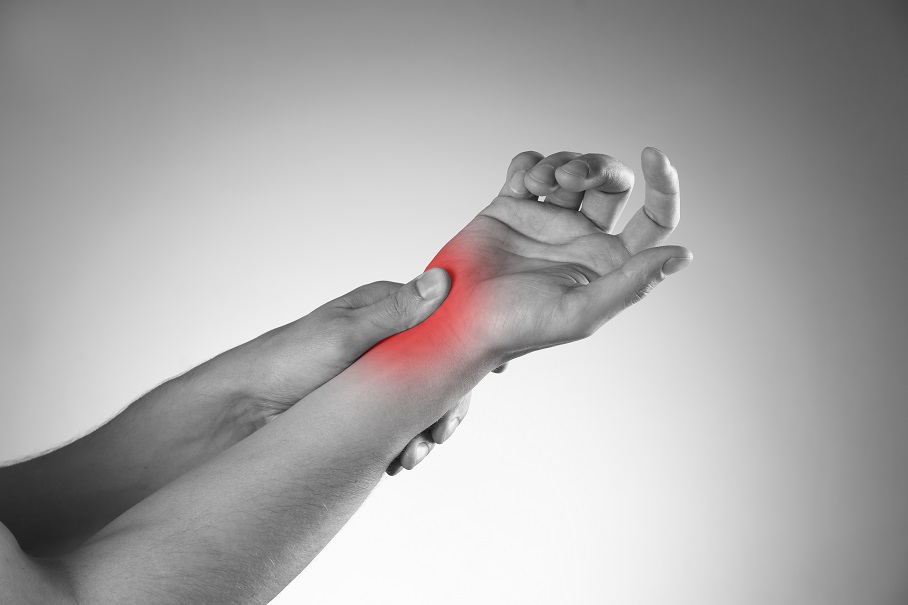
- 28 Feb 19El dolor crónico es un problema de salud importante, y se estima que la mitad de las personas que sufren de dolor crónico lo han tenido durante más de 10 años.1
- 31 Oct 18Tu periodo está retrasado, muy retrasado. No estás embarazada y no estás en la menopausia.
- 31 Mar 19Ahora, en pleno invierno de 2019 (1), podemos apostar a que la temporada de gripe y los síntomas alcanzarán su punto máximo. El clima frío hace que los humanos nos mantengamos en ambientes cerrados, lo que significa que nos toca aguantar las bacterias, los virus y otros patógenos de los demás con más frecuencia.
- 31 Oct 18La opinión del autor es que los vegetarianos no están condenados a tener una deficiencia de proteínas simplemente porque han cambiado de una dieta omnívora a una completamente basada en plantas.
Boletín
No se pudo guardar su suscripción. Inténtalo de nuevo.
Su suscripción ha sido exitosa.
Más popular
- 16 Jun 13
- 17 Jun 13
- 17 Jun 13
- 16 Jun 13
- 01 Jul 13
- 16 Jun 13
- 17 Jun 13
- 17 Jun 13
- 16 Jun 13
- 01 Jul 13
- 16 Jun 13
- 17 Jun 13
- 17 Jun 13
- 16 Jun 13
- 01 Jul 13